Алканы — номенклатура, получение, химические свойства. Алканы Конспект алканы химические свойства и способы получения
Строение алканов
Алканы - углеводороды, в молекулах которых атомы связаны одинарными связями и которые соответствуют общей формуле C n H 2n+2 . В молекулах алканов все атомы углерода находятся в состоянии sр 3 -гибридизации .
Это означает, что все четыре гибридные орбитали атома углерода одинаковы по форме, энергии и направлены в углы равносторонней треугольной пирамиды - тетраэдра . Углы между орбиталями равны 109° 28′. Вокруг одинарной углерод-углеродной связи возможно практически свободное вращение, и молекулы алканов могут приобретать самую разнообразную форму с углами при атомах углерода, близкими к тетраэдрическому (109° 28′), например, в молекуле н-пентан.

Особо стоит напомнить о связях в молекулах алканов. Все связи в молекулах предельных углеводородов одинарные. Перекрывание происходит по оси, соединяющей ядра атомов, т. е. это σ-связи . Связи углерод - углерод являются неполярными и плохо поляризуемыми. Длина С-С связи в алканах равна 0,154 нм (1,54 10 10 м). Связи С-Н несколько короче. Электронная плотность немного смещена в сторону более электроотрицательного атома углерода, т. е. связь С-Н является слабополярной .
Гомологический ряд метана
Гомологи - вещества, сходные по строению и свойствам и отличающиеся на одну или более групп СН 2 .


Предельные углеводороды составляют гомологический ряд метана.
Изомерия и номенклатура алканов
Для алканов характерна так называемая структурная изомерия . Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкан, для которого характерны структурные изомеры, - это бутан.
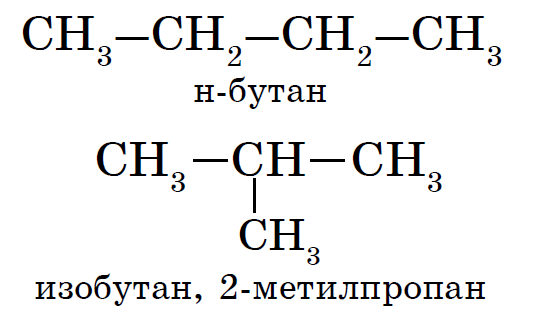
Рассмотрим подробнее для алканов основы номенклатуры ИЮПАК .
1. Выбор главной цепи . Формирование названия углеводорода начинается с определения главной цепи - самой длинной цепочки атомов углерода в молекуле, которая является как бы ее основой.
2. Нумерация атомов главной цепи . Атомам главной цепи присваивают номера. Нумерация атомов главной цепи начинается с того конца, к которому ближе стоит заместитель (структуры А, Б). Если заместители находятся на равном удалении от конца цепи, то нумерация начинается от того конца, при котором их больше (структура В). Если различные заместители находятся на равном удалении от концов цепи, то нумерация начинается с того конца, к которому ближе старший (структура Г). Старшинство углеводородных заместителей определяется по тому, в каком порядке следует в алфавите буква, с которой начинается их название: метил (-СН 3), затем пропил (-СН 2 -СН 2 -СН 3), этил (-СН 2 -СН 3) и т. д.
Обратите внимание на то, что название заместителя формируется заменой суффикса -ан на суффикс -ил в названии соответствующего алкана.
3. Формирование названия . В начале названия указывают цифры - номера атомов углерода, при которых находятся заместители. Если при данном атоме находятся несколько заместителей, то соответствующий номер в названии повторяется дважды через запятую (2,2-). После номера через дефис указывают количество заместителей (ди - два, три - три, тетра - четыре, пента - пять) и название заместителя (метил, этил, пропил). Затем без пробелов и дефисов - название главной цепи. Главная цепь называется как углеводород - член гомологического ряда метана (метан, этан, пропан и т. д.).




Названия веществ, структурные формулы которых приведены выше, следующие:
Структура А: 2-метилпропан;
Структура Б: 3-этилгексан;
Структура В: 2,2,4-триметилпентан;
Структура Г: 2-метил 4-этилгексан.
Отсутствие в молекулах предельных углеводородов полярных связей приводит к тому, что они плохо растворяются в воде , не вступают во взаимодействие с заряженными частицами (ионами) . Наиболее характерными для алканов являются реакции, протекающие с участием свободных радикалов .
Физические свойства алканов
Первые четыре представителя гомологического ряда метана - газы . Простейший из них - метан - газ без цвета, вкуса и запаха (запах «газа», почувствовав который, надо звонить 04, определяется запахом меркаптанов - серосодержащих соединений, специально добавляемых к метану, используемому в бытовых и промышленных газовых приборах для того, чтобы люди, находящиеся рядом с ними, могли по запаху определить утечку).
Углеводороды состава от С 5 Н 12 до С 15 Н 32 - жидкости; более тяжелые углеводороды - твердые вещества. Температуры кипения и плавления алканов постепенно увеличиваются с возрастанием длины углеродной цепи. Все углеводороды плохо растворяются в воде, жидкие углеводороды являются распространенными органическими растворителями.


Химические свойства алканов
Реакции замещения.
Наиболее характерными для алканов являются реакции свободнорадикального замещения , в ходе которого атом водорода замещается на атом галогена или какую-либо группу.
Приведем уравнения характерных реакций галогенирования :
В случае избытка галогена хлорирование может пойти дальше, вплоть до полного замещения всех атомов водорода на хлор :

Полученные вещества широко используются как растворители и исходные вещества в органических синтезах.
Реакция дегидрирования (отщепления водорода).
В ходе пропускания алканов над катализатором (Pt, Ni, Al 2 O 3 , Cr 2 O 3) при высокой температуре (400-600 °C) происходит отщепление молекулы водорода и образование алкена :
Реакции, сопровождающиеся разрушением углеродной цепи. Все предельные углеводороды горят с образованием углекислого газа и воды. Газообразные углеводороды, смешанные с воздухом в определенных соотношениях, могут взрываться.
1. Горение предельных углеводородов - это свободнорадикальная экзотермическая реакция, которая имеет очень большое значение при использовании алканов в качестве топлива:
В общем виде реакцию горения алканов можно записать следующим образом:
2. Термическое расщепление углеводородов .
Процесс протекает по свободнорадикальному механизму . Повышение температуры приводит к гомолитическому разрыву углерод-углеродной связи и образованию свободных радикалов.
Эти радикалы взаимодействуют между собой, обмениваясь атомом водорода, с образованием молекулы алкана и молекулы алкена :
Реакции термического расщепления лежат в основе промышленного процесса - крекинга углеводородов . Этот процесс является важнейшей стадией переработки нефти.
3. Пиролиз . При нагревании метана до температуры 1000 °С начинается пиролиз метана - разложение на простые вещества:
При нагревании до температуры 1500 °С возможно образование ацетилена :
4. Изомеризация . При нагревании линейных углеводородов с катализатором изомеризации (хлоридом алюминия) происходит образование веществ с разветвленным углеродным скелетом :

5. Ароматизация . Алканы с шестью или более углеродными атомами в цепи в присутствии катализатора циклизуются с образованием бензола и его производных:

Алканы вступают в реакции, протекающие по свободнорадикальному механизму, т. к. все атомы углерода в молекулах алканов находятся в состоянии sp 3 -гибридизации. Молекулы этих веществ построены при помощи ковалентных неполярных С-С (углерод - углерод) связей и слабополярных С-Н (углерод - водород) связей. В них нет участков с повышенной и с пониженной электронной плотностью, легко поляризуемых связей, т. е. таких связей, электронная плотность в которых может смещаться под действием внешних факторов (электростатических полей ионов). Следовательно, алканы не будут реагировать с заряженными частицами, т. к. связи в молекулах алканов не разрываются по гетеролитическому механизму.
Углеводороды, в молекулах которых атомы связаны одинарными связями и которые соответствуют общей формуле C n H 2 n
+2
.
В молекулах алканов все атомы углерода находятся в состоянии sр 3 -гибридизации. Это означает, что все четыре гибридные орбитали атома углерода одинаковы по форме, энергии и направлены в углы равносторонней треугольной пирамиды - тетраэдра. Углы между орбиталями равны 109° 28′.
Вокруг одинарной углерод-углеродной связи возможно практически свободное вращение, и молекулы алканов могут приобретать самую разнообразную форму с углами при атомах углерода, близкими к тетраэдрическому (109° 28′), например, в молекуле н -пентана.

Особо стоит напомнить о связях в молекулах алканов. Все связи в молекулах предельных углеводородов одинарные. Перекрывание происходит по оси,
соединяющей ядра атомов, т. е. это σ-связи. Связи углерод - углерод являются неполярными и плохо поляризуемыми. Длина С-С связи в алканах равна 0,154 нм (1,54 10 — 10 м). Связи С-Н несколько короче. Электронная плотность немного смещена в сторону более электроотрицательного атома углерода, т. е. связь С-Н является слабополярной.
Отсутствие в молекулах предельных углеводородов полярных связей приводит к тому, что они плохо растворяются в воде, не вступают во взаимодействие с заряженными частицами (ионами). Наиболее характерными для алканов являются реакции, протекающие с участием свободных радикалов.
Гомологический ряд метана
Гомологи - вещества, сходные по строению и свойствам и отличающиеся на одну или более групп СН 2 .

Изомерия и номенклатура
Для алканов характерна так называемая структурная изомерия. Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкан, для которого характерны структурные изомеры, - это бутан.
Основы номенклатуры
1. Выбор главной цепи.
Формирование названия углеводорода начинается с определения главной цепи - самой длинной цепочки атомов углерода в молекуле, которая является как бы ее основой.
2. Нумерация атомов главной цепи.
Атомам главной цепи присваивают номера. Нумерация атомов главной цепи начинается с того конца, к которому ближе стоит заместитель (структуры А, Б). Если заместители находятся на равном удалении от конца цепи, то нумерация начинается от того конца, при котором их больше (структура В). Если различные заместители находятся на равном удалении от концов цепи, то нумерация начинается с того конца, к которому ближе старший (структура Г). Старшинство углеводородных заместителей определяется по тому, в каком порядке следует в алфавите буква, с которой начинается их название: метил (-СН 3), затем этил (-СН 2 -СН 3), пропил (-СН 2 -СН 2 -СН 3) и т. д.
Обратите внимание на то, что название заместителя формируется заменой суффикса -ан на суффикс —ил
в названии соответствующего алкана.
3. Формирование названия
. В начале названия указывают цифры - номера атомов углерода, при которых находятся заместители. Если при данном атоме находятся несколько заместителей, то соответствующий номер в названии повторяется дважды через запятую (2,2-). После номера через дефис указывают количество заместителей (ди
- два, три
- три, тетра
- четыре, пента
- пять) и название заместителя (метил, этил, пропил). Затем без пробелов и дефисов - название главной цепи. Главная цепь называется как углеводород - член гомологического ряда метана (метан
СН 4 , этан
С 2 Н 6 , пропан
C 3 H 8 , С 4 Н 10, пентан
С 5 Н 12 , гексан
С 6 Н 14 , гептан
C 7 H 16, октан
C 8 H 18, нонан
С 9 Н 20, декан
С 10 Н 22).

Физические свойства алканов
Первые четыре представителя гомологического ряда метана - газы. Простейший из них - метан - газ без цвета, вкуса и запаха (запах «газа», почувствовав который, надо звонить 04, определяется запахом меркаптанов - серосодержащих соединений, специально добавляемых к метану, используемому в бытовых и промышленных газовых приборах для того, чтобы люди, находящиеся рядом с ними, могли по запаху определить утечку).
Углеводороды состава от С 4 Н 12 до С 15 Н 32 - жидкости; более тяжелые углеводороды - твердые вещества. Температуры кипения и плавления алканов постепенно увеличиваются с возрастанием длины углеродной цепи. Все углеводороды плохо растворяются в воде, жидкие углеводороды являются распространенными органическими растворителями.
Химические свойства алканов
Реакции замещения.
Наиболее характерными для алканов являются реакции свободнорадикального замещения, в ходе которого атом водорода замещается на атом галогена или какую-либо группу. Приведем уравнения характерных реакций галогенирования:
В случае избытка галогена хлорирование может пойти дальше, вплоть до полного замещения всех атомов водорода на хлор:
Полученные вещества широко используются как растворители и исходные вещества в органических синтезах.
Реакция дегидрирования
(отщепления водорода)
.
В ходе пропускания алканов над катализатором (Pt, Ni, А1 2 0 3 , Сг 2 0 3) при высокой температуре (400-600 °С) происходит отщепление молекулы водорода и образование алкена:
Реакции, сопровождающиеся разрушением углеродной цепи.
Все предельные углеводороды горят с образованием углекислого газа и воды. Газообразные углеводороды, смешанные с воздухом в определенных соотношениях, могут взрываться.
1. Горение предельных углеводородов
- это свободнорадикальная экзотермическая реакция, которая имеет очень большое значение при использовании алканов в качестве топлива:
В общем виде реакцию горения алканов можно записать следующим образом:
2. Термическое расщепление углеводородов.
Процесс протекает по свободнорадикальному механизму. Повышение температуры приводит к гомолитическому разрыву углерод-углеродной связи и образованию свободных радикалов.
Эти радикалы взаимодействуют между собой, обмениваясь атомом водорода, с образованием молекулы алкана и молекулы алкена:
Реакции термического расщепления лежат в основе промышленного процесса - крекинга углеводородов. Этот процесс является важнейшей стадией переработки нефти.
3. Пиролиз
. При нагревании метана до температуры 1000 °С начинается пиролиз метана - разложение на простые вещества:![]()
При нагревании до температуры 1500 °С возможно образование ацетилена:
4. Изомеризация
. При нагревании линейных углеводородов с катализатором изомеризации (хлоридом алюминия) происходит образование веществ с разветвленным углеродным скелетом:
5. Ароматизация
. Алканы с шестью или более углеродными атомами в цепи в присутствии катализатора циклизуются с образованием бензола и его производных:
Алканы вступают в реакции, протекающие по свободнорадикальному механизму, т. к. все атомы углерода в молекулах алканов находятся в состоянии sp 3 -гибридизации. Молекулы этих веществ построены при помощи ковалентных неполярных С-С (углерод - углерод) связей и слабополярных С-Н (углерод - водород) связей. В них нет участков с повышенной и с пониженной электронной плотностью, легко поляризуемых связей, т. е. таких связей, электронная плотность в которых может смещаться под действием внешних факторов (электростатических полей ионов). Следовательно, алканы не будут реагировать с заряженными частицами, т. к. связи в молекулах алканов не разрываются по гетеролитическому механизму.
Урок № 7.
Тема урока: «Природный газ. Алканы ».
Цели урока: 1) образовательная: обучающиеся должны усвоить: понятие о предельных углеводородах, их химическом, пространственном и электронном строении; на примере рассмотрения метана и его гомологов - электронную природу химических связей и пространственное строении молекул углеводородов; основные способы лабораторного и промышленного получения алканов; физические свойства предельных углеводородов.
2) развивающая: обучающиеся должны научиться: объяснять тетраэдричное строение молекулы метана, зигзагообразное строение цепи у предельных углеводородов; записывать молекулярные, структурные и электронные формулы предельных углеводородов, называть их по систематической номенклатуре и по названию составлять формулы;
3) воспитательная: обучающиеся должны убедиться: в мировоззренческих понятиях о познаваемости природы, причинно-следственной зависимости между составом, строением, свойствами и применением предельных углеводородов и др.; что природа химической связи одинакова как у веществ неорганических, так и органических, что является одним из доказательств единства этих веществ; в необходимости соблюдения правил пользования «бытовым» газом вследствие его взрывоопасности.
Основные понятия, изучаемые на уроке: предельные углеводороды, гомологи, гомологический ряд, гомологическая разность, общая формула, электронная формула, пространственное строение молекул веществ, тетраэдрическое строение молекул метана.
Планируемые результаты обучения: уметь на примере углеводородов ряда метана устанавливать, чем по составу молекул отличается каждый последующий углеводород от предыдущего; составлять структурные формулы первых 4-5 углеводородов этого ряда, приводить примеры изомеров этих веществ; определять молярную массу предельных углеводородов по их формулам, давать исторически сложившиеся названия; на конкретных примерах объяснять электронное и пространственное строение молекул предельных углеводородов и некоторых из их изомеров; составлять структурные и электронные формулы углеводородов по числу атомов углерода в молекуле и их моделям.
Метод: проблемная беседа с выдвижением гипотез; смоделировать проблемную ситуацию, чтобы затем выяснить причину закономерного изменения состава углеводородов на группу СН 2 , кажущегося нарушения валентности углерода, многообразия органических соединений; при объяснении материала по ходу урока демонстрация лабораторных опытов, которые требуются по программе.
Оборудование и реактивы: на демонстрационном столе набор углеводородов: нефть, бензин (керосин), пропан-бутановая смесь (сжиженный газ в баллончике), машинное масло, вазелин, парафин (свеча), изделия из полиэтилена; демонстрационные схемы образования ковалентных и ионных связей, разъемная модель тетраэдра, масштабные и шаростержневые модели молекул метана и других углеводородов; газовая зажигалка с прозрачным резервуаром; кристаллические CH 3 COONa, NaOH, КМnО 4 , прибор для получения газов, пробирки; таблица: углеводороды ряда метана; на ученических столах: наборы для моделирования молекул; модели молекул Стюарта - Бриглеба.
Ход урока.
1. Организационный момент.
2. Изучение нового материала.
I . Понятие углеводородов.
Преподаватель предлагает ребятам «расшифровать» термин углеводород. Это не представляет никакого труда: углеводородами называются органические соединения, состоящие из атомов двух элементов - углерода и водорода. Это самые простые органические вещества, что отнюдь не умаляет их значения. Напротив, по определению немецкого химика Карла Шорлеммера, «органическая химия есть химия углеводородов и их производных».
Общую формулу углеводородов можно представить в виде С x Н y , где х и у связаны между собой определенным соотношением, определяющим класс углеводорода. Единственный углеводород - метан -имеет в своем составе один атом углерода; в остальных углеводородах число х колеблется от двух до нескольких тысяч.
Общую классификацию органических веществ, рассмотренную в §5 учебника (см. рис. 1 данного пособия), можно распространить и на углеводороды. Преподаватель обращает внимание на то, что изучение углеводородов начинается с самого простого класса - ациклических предельных соединений, называемых алканами.
II . Электронное и пространственное строение молекулы метана.
Простейший углеводород - метан - известен людям очень давно. Его называли болотным или рудничным газом.
Атом углерода в метане находится в состоянии sp 3 -гибридизации. Обучающиеся вспоминают, что углерод в данном случае имеет четыре равноценные гибридные орбитали, оси которых направлены к вершинам правильного тетраэдра. Угол между осями этих орбиталей составляет 109°28". Преподаватель изображает на доске строение атома углерода в sp 3 -гибридном состоянии.
Важно подчеркнуть, что электронное строение атома углерода определяет пространственное расположение атомов в молекуле метана. Все четыре ковалентные связи С-Н образованы за счет перекрывания sp 3 -орбиталей атома углерода и s-орбитали водорода. Все связи в молекуле метана относятся к σ-типу. Центры ядер атомов водорода лежат в вершинах правильного тетраэдра, валентный угол Н-С-Н составляет 109°28.

Для более конкретного восприятия пространственной структуры метана преподаватель демонстрирует объемную модель молекулы (шаростержневую или Стюатра - Бриглеба), дает ребятам домашнее задание собрать аналогичную модель из спичек и пластилиновых шариков.
III . Гомологический ряд предельных углеводородов.
Эту часть урока преподаватель начинает с упоминания об уникальном свойстве атома углерода образовывать за счет связи друг с другом длинные цепочки. Если все оставшиеся валентности углерода при этом будут заняты атомами водорода, это и будут углеводороды, которые принято называть предельными, парафиновыми, насыщенными или алканами. Преподаватель дает определение алканов и расшифровывает значение всех синонимов.
Слово «предельные» означает, что атомы углерода связаны с максимальным (предельным) числом атомов водорода. Насыщенный углеводород не имеет в своем составе двойных или тройных углерод-углеродных связей. Термин «парафины» происходит от латинского словосочетания parum affinis , что означает не обладающий сродством.
Таким образом, предельные углеводороды составляют особую группу, класс органических соединений. При переходе к повторению понятия гомологического ряда, преподаватель проводит следующую аналогию. Любая область знания имеет раздел, называемый таксономией (дословно: располагать по порядку, по закону). Он занимается классификацией тех объектов, которые изучает данная наука. В биологии, например, типы животных делятся на классы, классы - на отряды, те - на семейства, которые подразделяются на рода, род делится на виды. В неорганической химии существует свое деление веществ на классы. Какие? Обучающиеся называют оксиды, основания, кислоты, соли. Внутри этих классов есть своя градация. В органической химии все вещества данного класса можно выстроить в ряд, называемый гомологическим. Пусть два атома углерода образовали друг с другом ковалентную неполярную связь. У каждого остается по три свободных валентности, неспаренных электрона. Если все эти валентные возможности насыщены атомами водорода, мы получим углеводород этан. Аналогично преподаватель строит молекулу пропана:
| | | | | | | | | |
– C – C – → H – C – C – H – C – C – C – → H – C – C – C – H
| | | | | | | | | |
Поскольку строение молекул подобно, похожи и их химические свойства. В чем различие в составе таких веществ? Из структурных формул хорошо видно, что они отличаются на группу – СН 2 – , одну или несколько.
Гомологическим рядом называется совокупность органических соединений, обладающих подобным строением и свойствами и отличающихся друг от друга по составу на одну или несколько групп – СН 2 – (гомологическая разность). Представители одного гомологического ряда называются гомологами.
С небольшой помощью учителя, «разделившего» молекулу пропана на фрагменты фигурными скобками, ребята выводят общую формулу алканов: С n Н 2 n +2 .
H – C – C – C – H
H + C n H 2n + H
Формулы этана и пропана, приведенные выше, называются полными структурными формулами . Чаще всего нет необходимости так подробно изображать структуру вещества. Вполне информативны сокращенные структурные формулы, в которых связи С- Н «свернуты», не показаны. Для упомянутых этана и пропана они выглядят привычно: СН 3 - СН 3 и СН 3 - СН 2 – СН 3 или даже СН 3 СН 3 и СН 3 СН 2 СН 3 . Важно подчеркнуть, что оба варианта равноценны. Ведь, как правило, преподаватель не придает особого значения тому или иному способу написания сокращенной структурной формулы, а ребята пытаются запомнить, нужен в формуле «штрих» или нет.
Еще один способ обозначения органических веществ - молекулярные формулы . Они показывают только состав молекулы, но не отражают порядок связей атомов. Этан имеет молекулярную формулу С 2 Н 6 , пропан - C 3 H 8 . Преподаватель проверяет, как ребята выполнили задание изготовить карточки с названиями и формулами первых 10 членов гомологического ряда алканов, просит приносить эти карточки на последующие уроки.
IV . Изомерия и номенклатура алканов.
Научить ребят составлять структурные формулы гомологов и изомеров - очень важная задача данного урока. К ее решению можно подойти таким способом. Преподаватель, пользуясь масштабными моделями молекул, предлагает вернуться к родоначальнику гомологического ряда алканов -метану. Все связи С-Н в молекуле равноценны. Если одну из этих связей разорвать таким образом, что каждый атом получит назад свой ранее обобществленный электрон, образуется две частицы: атом водорода и метальный радикал. Как называется такой разрыв связей в органической химии? Это гемолитический разрыв. Теперь соединим между собой два метальных радикала. Получим гомолог метана - этан. В этом углеводороде так же, как в метане, все атомы водорода эквивалентны. Заменой любого из них на метальный радикал получаем единственный третий гомолог состава С 3 Н 8 - пропан. Атомы водорода в этом алкане уже не одинаковы: шесть из них расположены у крайних углеродных атомов, а два - у среднего. Если мы формально заменим любой из шести «крайних» атомов Н на радикал СН 3 -, получим бутан нормального строения - н -бутан. Если такой замене подвергнуть один из двух «центральных» атомов водорода - это уже другая молекула, другое вещество того же состава С 4 Н 10 - изобутан. H H H H
H – C – C – C – C – H
H H H H H H | | | |
| | | | | | a H H H H
H – C–– H → H – C – C ––H → H – C – C – C–– H a
| | | | | б | H H H
H H H H H H | | |
H – C – C – C – H
Преподаватель спрашивает, как называются вещества, имеющие один и тот же состав, но различное химическое строение? Конечно же, это изомеры. И здесь еще раз закрепляются понятия о структурной изомерии.
Изомеры бутана имеют различный порядок связи атомов в молекуле . Это структурная изомерия .
Такой вид структурной изомерии, в котором представители одного гомологического ряда отличаются порядком связи атомов углерода в молекуле, называется изомерией углеродного скелета.
На примере изомеров пентана, построенных аналогично из н-бутана и изобутана, преподаватель закрепляет различие в понятиях «изомер» и «гомолог». Любой из двух бутанов по отношению к любому пентану - гомолог, но не изомер! Пентаны «доводятся» друг другу изомерами, но не являются гомологами.
Изомеры пентана Изомеры бутана
H H H H H H H H H H
| | | | | | | | | |
H – C – C – C – C – C – C – H H – C – C – C – C – H
| | | | | | | | | |
H H H H H H H H H H
гомологи
CH 3 – CH – CH 2 – CH 3 CH 3 – CH – CH 3
Гомологи
H – C – C – C – H
На данном этапе целесообразно ввести понятия первичного, вторичного, третичного и четвертичного атомов углерода на примере структур, изображенных на доске. Такая классификация проводится по числу соседних углеродных атомов, связанных с данным. Пентан нормального строения имеет два первичных и три вторичных атома углерода; изопентан - три первичных, один вторичный и один третичный атом; последний изомер - четыре первичных и один четвертичный атом углерода.
Для того чтобы обучающиеся при написании формул всех возможных изомеров указанного состава не изображали лишние структуры, а также избежали некоторых распространенных ошибок в номенклатуре алканов, полезно с применением модели молекулы (например, изопентана) пояснить следующее. Реальная молекула занимает в пространстве любое положение и форму, которую позволяет ей свободное вращение относительно связей С – С. Изобразить же ее структурную формулу на плоскости (на доске или в тетради) мы можем произвольным, удобным для нас способом. От этого изопентан не перестанет быть изопентаном, не превратится в другой изомер.
Это всё пентаны!
CH 3 CH 3 CH 3 CH 3
CH 3 – CH – CH 2 – CH 3 CH 3 – CH CH – CH 2 CH 2 – CH – CH 3 CH – C 2 H 5
CH 2 CH 3 CH 3 CH 3 CH 3 CH 3
Для того чтобы была однозначность в присвоении каждому веществу своего собственного имени, и по названию можно было воспроизвести формулу вещества, напоминает преподаватель, химики пользуются особой системой названий - химической номенклатурой, и подчеркивает, что, как уже знают обучающиеся, наиболее универсальна и понятна на любом языке так называемая международная номенклатура (IUPAC). Обучающиеся называют первую из изображенных структур и убеждаются, что и все остальные имеют то же самое название - 2-метилбутан. Это одно и то же вещество! Верно и обратное: каждому названию может соответствовать единственное вещество.
Преподаватель подчеркивает, что составлять названия алканов и по названию изображать структурные формулы - увлекательное занятие. Особенно если обучающиеся работают рационально. Для этого необходимо строго придерживаться следующего алгоритма.
1. Выбрать в молекуле самую длинную цепочку углеродных атомов.
2. Пронумеровать цепочку с того конца, к которому ближе разветвление молекулы.
3. Основа названия - название углеводорода с тем же числом углеродных атомов, что и в самой длинной цепи (помогает карточка-подсказка) .
4. Перед основой названия перечислить все заместители основной цепи с указанием номеров углеродных атомов, при которых они стоят. Если одинаковых заместителей несколько, перед их названиями ставят приставки ди-, три-, тетра- и т. д.
5. Все цифры друг от друга отделяются запятыми, буквы от цифр - дефисом, название пишется в одно слово (без пробелов). Если при одном углеродном атоме имеется не один, а два заместителя, его цифра повторяется в названии дважды (например, 2,2-диметилбутан, а не 2-диметилбутан).
Перечисленные правила иллюстрируются следующими примерами:
CH 3 – CH 2 – CH 2 – CH 2 – CH 2 – CH 3 CH 3 – CH – CH 2 – CH 2 – CH 3
н -гексан |
2-метилпентан
CH 3 – C – CH 3 CH 3 – CH 2 – C – CH – CH 3
2,2-диметилпропан 2,3,3-триметилпентан
7 6 5 4 | 3 3 4 |
CH 3 – CH 2 – CH – CH – CH – CH 3 CH 3 – CH – CH – CH 3
C 2 H 5 CH 2 – CH 3 C 2 H 5
3,4-диметил-5-этилгептан 3 , 4-диэтилгексан
Для особо интересующихся химией учащихся преподаватель напоминает, что часто при названии углеводородов и радикалов используют некоторые термины иной номенклатуры - рациональной. Полезно запомнить, что при наличии в алкане или алкильном заместителе фрагмента СН 3 -СН (СН 3) - к его названию можно добавить префикс изо- , фрагмента СН 3 -С(СН 3) 2 - префикс нео- :
CH 3 – CH – CH 3 CH 3 – C – CH 2 – CH 3
изобутан неогексан
CH 3 – CH – CH 2 – CH 3 – CH –
изобутил изопропил
Обучающиеся должны уметь составлять структурные формулы всех изомерных углеводородов предложенного им состава. Это требует определенного навыка.
Изображать формулы возможных изомеров следует, начиная с единственного изомера нормального строения. Затем, укорачивая цепочку последовательно на один углеродный атом, изображать формулы изомеров с разветвленным углеродным скелетом. Если на первых парах возникают ошибки в определении числа атомов водорода, лучше сначала нарисовать «голый» углеродный скелет (пересчитайте атомы углерода!), а затем «навесить» на него водородные атомы, учитывая четырёхвалентность атома углерода.
Как не написать «лишние» формулы изомеров? Нужно сразу называть изображенный алкан: двух одинаковых названий быть не должно.
Структурную формулу по названию изображать еще проще. Начинать нужно с основы названия - цепочки «голых» углеродных атомов, которую нумеруют слева направо. Затем размещают радикалы и наконец добавляют в цепочку атомы водорода, учитывая четырехвалентность атома углерода.
V . Способы получения алканов.
Преподаватель, опираясь на знания учащихся из курса неорганической химии, напоминает, что способы получения алканов, как и любых других практически значимых веществ, можно разделить на промышленные и лабораторные (рис. 3).
Способы получения алканов
Промышленные Лабораторные
Выделение Крегинг Изомерии- Гидриро- Реакция Пиролиз Гидролиз
из природ- нефтепро- зация вание Вюрца солей кар- карбида
ных источ- дуктов алканов алкенов боновых алюминия
ников кислот
Природный Нефть Попутные
газ нефтяные газы
Рис.3. Способы получения предельных углеводородов.
В промышленности, технике и быту индивидуальные (химически чистые) углеводороды используются нечасто. Вполне достаточно иметь смесь алканов, близких по молекулярной массе. Например, природный газ главным образом состоит из метана (88-95%), этана (3-8%), пропана (0,7-2%) и бутана (0,2-0,7%) с примесью неорганических газов. Для получения практически ценных веществ из нефти ее подвергают ректификации - разделению на фракции, что подробно описано в учебнике. Фракция - это смесь веществ, температуры кипения которых находятся в определенном заданном интервале.
Переходя к рассмотрению процессов промышленной переработки нефтепродуктов, преподаватель начинает с сообщения о том, что наиболее ценной фракцией прямой перегонки нефти является бензин. Однако выход этой фракции не превышает 17-20% от массы сырой нефти. Возникает проблема: как удовлетворить все возрастающие потребности общества в автомобильном и авиационном топливе? Решение было найдено в конце XIX в. русским инженером Владимиром Григорьевичем Шуховым. В 1891 г. он впервые осуществил промышленный крекинг керосиновой фракции нефти, что позволило увеличить выход бензина до 65-70% (в расчете на сырую нефть)! Только за разработку процесса термического крекинга нефтепродуктов благодарное человечество золотыми буквами вписало имя этого уникального человека в историю цивилизации. Однако немногие знают, что Шуховым в Саратове были созданы речные наливные баржи для перевозки нефти. Эти суда впервые в мире собирались из отдельных секций, что позволяло спускать их со стапелей в очень короткий срок. Для загрузки и разгрузки баржи В. Г. Шухов использовал не мускульную силу, как было до тех пор, а паровые насосы. На бакинских нефтяных промыслах Владимир Григорьевич изобрел первый трубопровод для перекачки нефти с подогревом, это позволило избежать кристаллизации парафина на стенках труб и образования парафиновых пробок.
Процесс изомеризации алканов нормального строения называется также риформингом. Он имеет очень большое значение для повышения качества бензиновой фракции, получаемой после первичной перегонки сырой нефти. Каталитическая изомеризация протекает по ионному механизму.
Преподаватель завершает рассмотрение промышленных способов получения алканов проблемной ситуацией. Добыча и потребление нефти уже давно превратились из чисто экономического вопроса в особую форму межгосударственных политических отношений. Казалось бы, нефтедобывающим странам экономически выгодно наращивание добычи и продажи нефти. Однако в этом случае цены на сырье упадут и вместо прибыли будут приносить убытки. Каждое государство имеет определенную квоту на объем продажи «черного золота», которая является предметом острейшей борьбы крупнейших нефтяных монополий и ведущих промышленно развитых стран.
Вместе с тем добыча и потребление нефти ежегодно увеличивается в среднем на 8%. По оценкам специалистов разведанных запасов хватит только на ближайшие 50-70 лет. Нельзя ли использовать современные растительные и животные остатки для производства если не нефти, то хотя бы газа (он называется биогазом )? Оказывается, это вполне возможно и уже в значительных масштабах используется во многих развивающихся странах (Индия, Китай). На заводах по производству биогаза в качестве сырья используются отходы животного и растительного происхождения, которые перегнивают в генераторах под действием анаэробных бактерий (рис. 4). Подобно природному газу, биогаз состоит главным образом из метана. Его можно использовать непосредственно для отопления жилищ, приготовления пищи или получения электроэнергии с помощью электрогенератора. Остатки растительных и животных отходов после получения биогаза могут использоваться в качестве высокоэффективных экологически чистых удобрений, т. к. содержат значительное количество
связанного азота.
Генератор
Растительная
биомасса
или навоз
генератор
Удобрения
Рис. 4. Получение и использование биогаза.
Из лабораторных способов получения алканов наиболее часто в задачах различного типа встречается синтез Вюрца и пиролиз солей карболовых кислот со щелочами.
Французский химик, член Парижской академии наук Шарль Адольф Вюрц в 1855 г. разработал универсальный способ синтеза предельных углеводородов нагреванием галогеналканов с металлами (натрием, цинковой пылью). Кстати, помимо приведенной реакции Ш. Вюрц внес огромный вклад в развитие органической химии, в его честь назван минерал вюрцит.
Для наглядности в уравнении реакции Вюрца преподаватель показывает, как под действием металла образуются радикалы, которые соединяются между собой в молекулу нового алкана. Этот процесс удобно изобразить и с помощью моделей молекул.
CH 3 – CH 2 – Br Br – CH 2 – CH 3 CH 3 – CH 2 – CH 2 – CH 3 + 2NaBr
Сильным учащимся, очевидно, будет по силам решить проблемную ситуацию: «Какие вещества получатся, если в реакцию Вюрца ввести два различных галогеналкана?» Очевидно, возможны три различных комбинации двух галогеналканов, которые должны привести к синтезу трех конечных углеводородов:
CH 3 –Br Br – CH 3 CH 3 – CH 3
CH 3 – CH 2 – CH 3
CH 3 – CH 2 – Br Br – CH 2 – CH 3 CH 3 – CH 2 – CH 2 – CH 3
Более сложна для учащихся обратная задача, например: какой галогеналкан следует взять в реакцию Вюрца, чтобы получить 2,3-диметилбутан? Решение лучше осуществлять от обратного:
Изобразить формулу требуемого продукта
СН 3 – СН – СН – СН 3
Разделить ее пополам (на два радикала)
СН 3 – СН – – СН – СН 3
Добавить к радикалам атом галогена
СН 3 – СН – Вr СН 3 – СНВr – СН 3
Это 2-бромпропан:
2CH 3 – CHBr – CH 3 + 2Na СН 3 – СН – СН – СН 3 + 2NaBr
Замечательная особенность реакции Вюрца - удвоение числа атомов углерода в продукте по сравнению с исходным веществом.
Особенность другого лабораторного способа получения алка-нов состоит в уменьшении числа углеродных атомов на единицу. Речь идет о пиролизе (нагревании вещества, приводящем к его разложению) солей карбоновых кислот со щелочью. Преподаватель демонстрирует эту реакцию, нагревая в пробирке с газоотводной трубкой смесь ацетата натрия с гидроксидом натрия. Обучающиеся констатируют, что метан нерастворим в воде (его можно собрать в пробирку методом вытеснения воды), не обесцвечивает раствор перманганата калия, горит бледно-голубым пламенем.
CH 3 – COONa + Na – O – H CH 4 + Na 2 CO 3
Написав на доске левую половину уравнения, преподаватель предлагает ребятам определить, какое неорганическое вещество (обведенное в рамочку) выделяется в качестве побочного продукта (карбонат натрия). Можно вспомнить, что функциональная группа карбоновых кислот называется карбоксильной. В этой реакции производное карбоновой кислоты (соль) теряет карбоксильный фрагмент, поэтому реакция называется декарбоксилированием.
Примером специфического способа получения алканов является гидролиз карбида алюминия. Этимология слова гидролиз (от греческого слов hydor- вода и lysis- разложение, распад) позволяет определить такие реакции, как процесс разложения сложного соединения на два или более новых вещества под действием воды.
Al 4 C 3 + 12H 2 O → 4Al (OH) 3 + 3CH 4
VI . Физические свойства алканов.
Преподаватель обращает внимание ребят на то, что в любом гомологическом ряду с увеличением числа атомов углерода в цепи (т. е. с увеличением относительной молекулярной массы) возрастают температуры плавления, кипения, плотность веществ. Это одно из подтверждений закона природы о переходе количества в качество. Таким образом, алканы могут существовать в трех различных агрегатных состояниях. Обучающиеся вспоминают типы агрегатных состояний, различия между ними с точки зрения межмолекулярного взаимодействия и степени упорядоченности молекул. Преподаватель на доске обобщает ответы, записывая схему (рис. 5).
Агрегатные состояния вещества
Газообразное Жидкое Твердое
Кристаллическое Аморфное
Рис. 5. Агрегатные состояния вещества.
Преподаватель демонстрирует образцы алканов. Газообразный углеводород увидеть непросто, но в газовой зажигалке под давлением пропан и бутан являются бесцветными жидкостями. При нажатии на клапан на волю с легким шипением вырываются бесцветные газообразные алканы, практически лишенные запаха. Если зажечь зажигалку, то алканы горят слегка окрашенным пламенем.
Жидкие предельные углеводороды (бензин) уже имеют запах. Преподаватель приливает несколько миллилитров бензина в пробирку с водой. Границу раздела видно плохо, обе жидкости бесцветны. При интенсивном встряхивании пробирки образуется мутная эмульсия, которая быстро расслаивается: предельные углеводороды нерастворимы в воде. Если бросить в пробирку кристаллик перманганата калия, водный слой окрасится. Окраска не исчезнет, поскольку алканы не реагируют с водным раствором КМnО 4 .
Вазелин - смесь жидких и твердых предельных углеводородов. Можно убедиться, что алканы с большой молекулярной массой жирные на ощупь. Парафин - смесь твердых углеводородов, имеет аморфное состояние. Преподаватель показывает, что кусочек парафина плавает на поверхности воды (его плотность меньше единицы) и легко плавится (при нагревании воды в пробирке кусочек парафина превратится в жидкость). Однако предельные углеводороды легко растворяются в неполярных органических растворителях, жидкие алканы смешиваются друг с другом.
Все газообразные и жидкие алканы образуют взрывоопасные смеси с воздухом, поэтому в быту с ними надо обращаться очень осторожно.
Для закрепления материала рекомендуется решить ряд задач на способы получения алканов, а также вспомнить задачи на нахождение формулы вещества по массовым долям элементов (алгоритм решения приведен в книге для учителя, 9 класс, глава «Органические вещества», а также ниже).
Алгоритм решения задач на вывод формулы вещества.
1. Обозначить формулу вещества с помощью индексов х, у, z и т. д. по числу элементов в молекуле.
2. Если в условии не дана массовая доля одного элемента, вычислить ее как разность 100% и массовых долей всех остальных элементов.
3. Найти отношение индексов х: у: z как отношение частных от деления массовой доли элемента на его относительную атомную массу. Привести частные от деления к отношению целых чисел. Определите простейшую формулу вещества.
4. В задачах на нахождение формул органических веществ часто требуется сравнить относительную молекулярную массу простейшей формулы с М r истинной, найденной по условию задачи (чаще всего плотности по воздуху или по водороду). Отношение этих масс дает число, на которое надо умножить индексы простейшей формулы.
Пример. Углеводород, плотность паров которого по водороду равна 15, содержит 80,0% углерода. Найдите его молекулярную формулу.
Дано: Решение:
ω (С) = 80,0% 1. Обозначим формулу углеводорода С х Ну.
Dн 2 (в-ва) = 15 2. Вычислим массовую долю водорода в соединении:
ω (Н) = 100% – ω (С) = 100% – 80,0% = 20,0%
Формула - ? 3. Найдем отношение индексов х: у
ω (С) ω (Н) 80,0 20,0 6,67 20,0
х: у = --- : --- = --- : --- = 6,67: 20 = --- : --- = 1: 3
А r (С) А r (Н) 12 1 6,67 6,67
Простейшая формула соединения СН 3 .
4. Рассчитаем относительную молекулярную массу углеводорода:
М r (С x H y) = 2 Dн 2 (в-ва) = 2 15 = 30
Сравним ее с относительной молекулярной массой простейшей формулы:
М r (СН 3) = 12 + 3=15
М r (С x H y) 30
Выяснили, что число атомов обоих элементов в простейшей формуле надо увеличить в два раза. Истинная формула вещества С 2 Н 6 .
3.Закрепление пройденного материала .
Усвоение учащимися материала данного урока очень важно, поскольку это основа успешного постижения номенклатуры и изомерии остальных классов органических соединений. Необходимо отработать основные типы заданий в классе и дома, только после этого можно переходить к изучению дальнейшего материала.
Задание 1.
1-й уровень.
1 . Какая из приведенных общих формул углеводородов соответствует алканам:
C n H 2n-2 ; C n H 2n ; C n H 2n+2 ; C n H 2n-6 ?
2 . Составьте структурные формулы предельных углеводородов по приведенным углеродным скелетам:
C – C – C – C C – C C C – C – C – C – C
C – C – C C C – C
C C – C – C – C – C
C – C – C C C C
3 . Какие углеводороды являются гомологами бутана: метан, этилен, изобутан, бензол, пентан?
4 . Напишите молекулярные формулы углеводородов: пропана, гексана, октана; радикалов: метила, этила,
2-й уровень.
1 . Укажите формулы алканов и назовите эти вещества:
С 6 Н 12 , С 4 Н 10 , С 2 Н 6 , С 13 Н 26 , С 6 Н 6 , С 9 Н 20 .
2 . Какие из перечисленных углеводородов содержат третичный атом углерода: этан, 2-метилбутан,
3,3-диметилпентан, 2,3-диметилгексан?
3. В каком состоянии гибридизации все атомы углерода в алканах: sp 2 -, sp -, sp 3 - ?
4 . Укажите пары гомологов: этан и этилен; пропан и этан; бутан и изобутан; гексан и гептан; метан и
Задание 2.
1-й уровень.
1 . Составьте структурные формулы изомеров пентана и назовите их.
2 . Назовите по международной номенклатуре следующие предельные углеводороды:
CH 3 – CH 2 – CH 2 СН 3 – СН – СН 2 – СН – СН 3 CH 3 – CH 2 – CH – CH 2 – CH 3
СН 3 СН 3 СН 3 C 2 H 5
3 . У каких алканов отсутствуют изомеры: метан, этан, пропан, бутан?
2-й уровень.
1 . Составьте структурные формулы всех изомеров гексана и назовите их.
2 . Составьте структурные формулы всех изомеров октана, имеющих один четвертичный атом углерода, и
назовите их.
3 . Напишите структурные формулы всех изомеров алкана, плотность паров которого по воздуху 2,48.
Задание 3.
Составьте структурные формулы следующих алканов:
1-й уровень. 2-метилгексан; З-метил-3-этилпентан; 2,3,4 - триметилгексан.
2-й уровень. 2,2,3,4-тетраметилгептан; 2,3-диметил-З-изопропилгексан; 2-метил-3,3-диэтилоктан.
Задание 4.
1-й уровень.
Объемные доли компонентов природного газа одного из месторождений составляют: 92% метана, 5% этана, 2% пропана, 0,7% оксида углерода (IV) и 0, 3% азота. Определите объемы каждого углеводорода в 120 м 3 природного газа.
2-й уровень.
Объемные доли алканов в природном газе равны: метан - 91%, этан - 6%, пропан - 2%, бутан - 1 %. Вычислите массовые доли газов и рассчитайте объем воздуха, который потребуется для сжигания 1 м 3 природного газа такого состава (условия нормальные, объемная доля кислорода в воздухе 20%).
Задание 5.
1-й уровень.
1 . Какие продукты получаются при крекинге предельного углеводорода состава С 14 Н 30 (тетрадекан)?
2 . Какие вещества получатся при нагревании с натрием следующих веществ: а) иодметан;
б) 1-бромпропан.
3 . Напишите уравнение реакции изомеризации н -бутана.
4 . Какие вещества получатся при нагревании пропионата натрия СН 3 -СН 2 -COONa с гидроксидом натрия? Напишите уравнение реакции.
2-й уровень.
1 . Напишите уравнение крекинга следующих алканов: а) н -декан; б) 2,3-диметилбутан.
2 . Напишите реакции Вюрца, с помощью которых можно получить следующие углеводороды:
а) н -гексан; б) 2,5-диметилгексан.
3 . При изомеризации предельного углеводорода нормального строения образуется 2,2,4-триметилпентан.
Определите исходный углеводород.
4 . Составьте уравнения реакций получения указанных углеводородов нагреванием соли
соответствующей кислоты со щелочью: а) пропан; б) 2-метилпропан.
Задание 6.
1-й уровень.
1. Вычислите массовые доли углерода в четырех первых представителях гомологического ряда алканов.
2 . Определите формулу углеводорода, массовая доля углерода в котором 75%, а водорода - 25%.
2-й уровень.
1 . Вычислите массовые доли водорода в четырех первых представителях гомологического ряда алканов.
Сделайте вывод о дальнейшем изменении массовой доли водорода следующих гомологов.
2. Массовая доля углерода в углеводороде составляет 82,76%. При нормальных условиях 10 л этого газа
имеют массу 25,88 г. Составьте структурные формулы изомеров углеводорода и назовите их по
международной номенклатуре.
4. Домашнее задание: § 11 с.67 - 72, упр. 1-6 с. 81; повт. § 10.
Методическая литература
Габриелян О.С., Остроумов И.Г. Настольная книга учителя. Химия. 10 кл. – М.: Дрофа, 2004.
Габриелян О.С., Рунов Н.Н., Толкунов В.И. Химический эксперимент в школе. 10 класс. М.: Дрофа, 2005.
Габриелян О.С., Попкова Т.Н., Карцова А.А. Органическая химия, 10: профильный уровень: методическое пособие: книга для учителя. М.: Просвещение, 2006.
Нагревание натриевой соли уксусной кислоты (ацетата натрия) с избытком щелочи приводит к отщеплению карбоксильной группы и образованию метана:
СН3СОNа + NаОН СН4 + Nа2С03
Если вместо ацетата натрия взять пропионат натрия, то образуется этан, из бутаноата натрия - пропан и т. д.
RСН2СОNа +NаОН -> RСН3 + Nа2С03
5. Синтез Вюрца. При взаимодействии галогеналканов с щелочным металлом натрием образуются предельные углеводороды и галогенид щелочного металла, например:
Действие щелочного металла на смесь галогенуглеводородов (например, бромэтана и бромметана) приведет к образованию смеси алканов (этана, пропана и бутана).
Реакция, на которой основан синтез Вюрца, хорошо протекает только с галогеналканами, в молекулах которых атом галогена присоединен к первичному атому углерода.
6. Гидролиз карбидов. При обработке некоторых карбидов, содержащих углерод в степени окисления -4 (например, карбида алюминия), водой образуется метан:
Аl4С3 + 12Н20 = ЗСН4 + 4Аl(ОН)3 Физические свойства
Первые четыре представителя гомологического ряда метана - газы. Простейший из них - метан - газ без цвета, вкуса и запаха (запах «газа», почувствовав который надо звонить по телефону 04, определяется запахом меркаптанов - серусодер-жащих соединений, специально добавляемых к метану, используемому в бытовых и промышленных газовых приборах, для того чтобы люди, находящиеся рядом с ними, могли по запаху определить утечку).
Углеводороды состава от С5Н12 до С15Н32 - жидкости, более тяжелые углеводороды - твердые вещества.
Температуры кипения и плавления алканов постепенно увеличиваются с возрастанием длины углеродной цепи. Все углеводороды плохо растворяются в воде, жидкие углеводороды являются распространенными органическими растворителями.
Химические свойства
1. Реакции замещения. Наиболее характерными для ал-канов являются реакции свободнорадикального замещения, в ходе которых атом водорода замещается на атом галогена или какую-либо группу.
Приведем уравнения наиболее характерных реакций.
Галогенирование:
СН4 + С12 -> СН3Сl + HCl
В случае избытка галогена хлорирование может пойти дальше, вплоть до полного замещения всех атомов водорода на хлор:
СН3Сl + С12 -> HCl + СН2Сl2
дихлорметан хлористый метилен
СН2Сl2 + Сl2 -> HCl + CHCl3
трихлорметан хлороформ
СНСl3 + Сl2 -> HCl + ССl4
тетрахлорметан четыреххлористый углерод
Полученные вещества широко используются как растворители и исходные вещества в органических синтезах.
2. Дегидрирование (отщепление водорода). При пропускании алканов над катализатором (Pt, Ni, А1203, Сг2O3) при высокой температуре (400-600 °С) происходит отщепление молекулы водорода и образование алкена:
СН3-СН3 -> СН2=СН2 + Н2
3. Реакции, сопровождающиеся разрушением углеродной цепи. Все предельные углеводороды горят с образованием углекислого газа и воды. Газообразные углеводороды, смешанные с воздухом в определенных соотношениях, могут взрываться. Горение предельных углеводородов - это свободнора-дикальная экзотермическая реакция, которая имеет очень большое значение при использовании алканов в качестве топлива.
СН4 + 2O2 -> С02 + 2Н2O + 880кДж
В общем виде реакцию горения алканов можно записать следующим образом:

Реакции термического расщепления лежат в основе промышленного процесса - крекинга углеводородов. Этот процесс является важнейшей стадией переработки нефти.
При нагревании метана до температуры 1000 °С начинается пиролиз метана - разложение на простые вещества. При нагревании до температуры 1500 °С возможно образование ацетилена.
4. Изомеризация. При нагревании линейных углеводородов с катализатором изомеризации (хлоридом алюминия) происходит образование веществ с разветвленным углеродным скелетом:
5. Ароматизация. Алканы с шестью или более углеродными атомами в цепи в присутствии катализатора циклизуются с образованием бензола и его производных:
В чем причина того, что алканы вступают в реакции, протекающие по свободнорадикальному механизму? Все атомы углерода в молекулах алканов находятся в состоянии sр 3 -гибридизации. Молекулы этих веществ построены при помощи ковалентных неполярных С-С (углерод-углерод) связей и слабополярных С-Н (углерод-водород) связей. В них нет участков с повышенной и пониженной электронной плотностью, легко поляризуемых связей, т. е. таких связей, электронная плотность в которых может смещаться под действием внешних воздействий (электростатических полей ионов). Следовательно, алканы не будут реагировать с заряженными частицами, так как связи в молекулах алканов не разрываются по гетеролитическому механизму.
Наиболее характерными реакциями алканов являются реакции свободнорадикального замещения. В ходе этих реакций атом водорода замещается на атом галогена или какую-либо группу.
Кинетику и механизм свободнорадикальных цепных реакций, т. е. реакций, протекающих под действием свободных радикалов - частиц, имеющих неспаренные электроны, - изучал замечательный русский химик Н. Н. Семенов. Именно за эти исследования ему была присуждена Нобелевская премия по химии .
Обычно механизм реакции свободнорадикального замещения представляют тремя основными стадиями:
1. Инициирование (зарождение цепи, образование свободных радикалов под действием источника энергии - ультрафиолетового света, нагревания).
2. Развитие цепи (цепь последовательных взаимодействий свободных радикалов и неактивных молекул, в результате которых образуются новые радикалы и новые молекулы).
3. Обрыв цепи (объединение свободных радикалов в неактивные молекулы (рекомбинация), «гибель» радикалов, прекращение развития цепи реакций).
Научные исследования Н.Н. Семенова
Семенов Николай Николаевич
(1896 - 1986)

Советский физик и физикохимик, академик. Лауреат Нобелевской премии (1956). Научные исследования относятся к учению о химических процессах, катализе, цепных реакциях, теории теплового взрыва и горении газовых смесей.
Рассмотрим этот механизм на примере реакции хлорирования метана:
СН4 + Сl2 -> СН3Сl + НСl
Инициирование цепи происходит в результате того, что под действием ультрафиолетового облучения или при нагревании происходит гомолитический разрыв связи Сl-Сl и молекула хлора распадается на атомы:
Сl: Сl -> Сl· + Сl·
Образовавшиеся свободные радикалы атакуют молекулы метана, отрывая у них атом водорода:
СН4 + Сl· -> СН3· + НСl
и превращая в радикалы СН3·, которые, в свою очередь, сталкиваясь с молекулами хлора, разрушают их с образованием новых радикалов:
СН3· + Сl2 -> СН3Сl + Сl· и т. д.
Происходит развитие цепи.
Наряду с образованием радикалов происходит их «гибель» в результате процесса рекомбинации - образования неактивной молекулы из двух радикалов:
СН3· + Сl· -> СН3Сl
Сl· + Сl· -> Сl2
СН3· + СН3· -> СН3-СН3
Интересно отметить, что при рекомбинации выделяется ровно столько энергии, сколько необходимо для разрушения только что образовавшейся связи. В связи с этим рекомбинация возможна только в том случае, если в соударении двух радикалов участвует третья частица (другая молекула, стенка реакционного сосуда), которая забирает на себя избыток энергии. Это дает возможность регулировать и даже останавливать свободнорадикальные цепные реакции.
Обратите внимание на последний пример реакции рекомбинации - образование молекулы этана. Этот пример показывает, что реакция с участием органических соединений представляет собой достаточно сложный процесс, в результате которого, наряду с основным продуктом реакции, очень часто образуются побочные продукты, что приводит к необходимости разрабатывать сложные и дорогостоящие методики очистки и выделения целевых веществ.
В реакционной смеси, полученной при хлорировании метана, наряду с хлорметаном (СН3Сl) и хлороводородом, будут содержаться: дихлорметан (СН2Сl2), трихлорметан (СНСl3), тетрахлорметан (ССl4), этан и продукты его хлорирования.
Теперь попытаемся рассмотреть реакцию галогенирования (например, бромирования) более сложного органического соединения - пропана.
Если в случае хлорирования метана возможно только одно моно-хлорпроизводное, то в этой реакции может образоваться уже два монобромпроизводных:
Видно, что в первом случае происходит замещение атома водорода при первичном атоме углерода, а во втором - при вторичном. Одинаковы ли скорости этих реакций? Оказывается, что в конечной смеси преобладает продукт замещения атома водорода, который находится при вторичном углероде, т. е. 2-бромпропан (СН3-СНВг-СН3). Давайте попытаемся объяснить это.
Для того чтобы это сделать, нам придется воспользоваться представлением об устойчивости промежуточных частиц. Вы обратили внимание, что при описании механизма реакции хлорирования метана мы упомянули радикал метил - СН3·? Этот радикал является промежуточной частицей между метаном СН4 и хлорметаном СН3Сl. Промежуточной частицей между пропаном и 1-бромпропаном является радикал с неспаренным электроном при первичном углероде, а между пропаном и 2-бромпропаном - при вторичном.
Радикал с неспаренным электроном при вторичном атоме углерода (б) является более устойчивым по сравнению со свободным радикалом с неспаренным электроном при первичном атоме углерода (а). Он и образуется в большем количестве. По этой причине основным продуктом реакции бромирования пропана является 2-бром-пропан - соединение, образование которого протекает через более устойчивую промежуточную частицу.
Приведем несколько примеров свободнорадикальных реакций:
Реакция нитрования (реакция Коновалова)![]()
Реакция применяется для получения нитросоединений - растворителей, исходных веществ для многих синтезов.
Каталитическое окисление алканов кислородом
Эти реакции являются основой важнейших промышленных процессов получения альдегидов, кетонов, спиртов непосредственно из предельных углеводородов, например:
СН4 + [О] -> СН3ОН
Применение
Предельные углеводороды, в особенности метан, находят очень широкое применение в промышленности (схема 2). Они являются простым и достаточно дешевым топливом, сырьем для получения большого количества важнейших соединений.
Соединения, полученные из метана, самого дешевого углеводородного сырья, применяют для получения множества других веществ и материалов. Метан используют как источник водорода в синтезе аммиака, а также для получения синтез-газа (смесь СО и Н2), применяемого для промышленного синтеза углеводородов, спиртов, альдегидов и других органических соединений.
Углеводороды более высококипящих фракций нефти используются как горючее для дизельных, турбореактивных двигателей, как основа смазочных масел, как сырье для производства синтетических жиров и т. д.
Приведем несколько промышленно значимых реакций, протекающих с участием метана. Метан используют для получения хлороформа, нитрометана, кислородсодержащих производных. Спирты, альдегиды, карбоновые кислоты могут образовываться при непосредственном взаимодействии алканов с кислородом в зависимости от условий проведения реакций (катализатора, температуры, давления):
Как вы уже знаете, углеводороды состава от С5Н12 до С11Н24 входят в бензиновую фракцию нефти и применяются в основном как горючее для двигателей внутреннего сгорания. Известно, что наиболее ценными компонентами бензина являются изомерные углеводороды, так как они обладают максимальной детонационной устойчивостью.
Углеводороды при контакте с кислородом воздуха медленно образуют с ним соединения - перекиси. Это медленно протекающая свободнорадикальная реакция, инициатором которой является молекула кислорода:
Обратите внимание на то, что гидропероксидная группа образуется при вторичных атомах углерода, которых больше всего в линейных, или нормальных, углеводородах.
При резком повышении давления и температуры, происходящем в конце такта сжатия, начинается разложение этих перекисных соединений с образованием большого числа свободных радикалов, которые «запускают» свободнорадикальную цепную реакцию горения раньше, чем это необходимо. Поршень еще идет вверх, а продукты горения бензина, которые уже успели образоваться в результате преждевременного поджига смеси, толкают его вниз. Это приводит к резкому уменьшению мощности двигателя, его износу.
Таким образом, основной причиной детонации является наличие перекисных соединений, способность образовывать которые максимальна у линейных углеводородов.
Наименьшей детонационной устойчивостью среди углеводородов бензиновой фракции (С5Н14 - С11Н24) обладает к-гептан. Наиболее устойчив (т. е. в наименьшей степени образует перекиси) так называемый изооктан (2,2,4-триметилпентан).
Общепринятой характеристикой детонационной устойчивости бензина является октановое число. Октановое число 92 (например, бензин А-92) означает, что данный бензин обладает теми же свойствами, что и смесь, состоящая из 92% изооктана и 8% гептана.
В заключение можно добавить, что использование высокооктанового бензина дает возможность повысить степень сжатия (давление в конце такта сжатия), что приводит к повышению мощности и КПД двигателя внутреннего сгорания.
Нахождение в природе и получение
На сегодняшнем уроке вы познакомились с таким понятием, как алканы, а также узнали о его химическом составе и методах получения. Поэтому давайте сейчас более подробно остановимся на теме нахождения алканов в природе и узнаем, как и где алканы нашли применение.
Главными источниками для получения алканов являются природный газ и нефть. Они составляют основную часть продуктов от нефтипереботки. Распространенный, в залежах осадочных пород метан, также является газовым гидратом алканов.
Основной составляющей природного газа является метан, но в его составе присутствует и небольшая доля этана, пропана и бутана. Метан можно обнаружить в выделениях угольных пластов, болот и в попутных нефтяных газах.
Также анканы можно получить методом коксования каменного угля. В природе встречаются и так называемые твердые алканы – озокериты, которые представлены в виде залежей горного воска. Озокерит можно обнаружить в восковых покрытиях растений или их семян, а также в составе пчелиного воска.
Промышленное выделение алканов берется из природных источников, которые к счастью пока неисчерпаемые. Их получают методом каталитического гидрирования оксидов углерода. Также метан можно получить в лабораторных условиях, используя метод нагревания ацетата натрия с твердой щелочью или гидролизом некоторых карбидов. Но и также алканы можно получить способом декарбоксилирования карбоновых кислот и при их электролизе.
Применение алканов
Алканы на бытовом уровне, широко применяются во многих сферах деятельности человека. Ведь очень сложно представить нашу жизнь без природного газа. И ни для кого не будет секретом, что основой природного газа является метан, из которого производят технический углерод, используемый при производстве топографических красок и шин. Холодильник, который есть в доме у каждого, также работает благодаря соединениям алканов, применяющихся в качестве хладагентов. А полученный из метана ацетилен используют для сварки и резки металлов.
Теперь вы уже знаете, что алканы используются как топливо. Они присутствуют в составе бензина, керосина, солярового масла и мазута. Кроме этого, они есть и в составе смазочных масел, вазелина и парафина.
В качестве растворителя и для синтеза различных полимеров, широкое применение нашел циклогексан. А в наркозе используют циклопропан. Сквалан, как высококачественное смазочное масло, является компонентом многих фармацевтических и косметических препаратов. Алканы являются сырьем, с помощью которого получают такие органические соединения, как спирт, альдегиды и кислоты.
Парафин является смесью высших алканов, а так как он нетоксичен, то широко используется в пищевой промышленности. Его применяют для пропитки упаковок для молочной продукции, соков, круп и так далее, но в том числе и при изготовлении жевательных резинок. А разогретый парафин используют в медицине при парафинолечении.
Помимо выше сказанного, парафином пропитаны головки спичек, для их лучшего горения, карандаши и из него изготавливают свечи.
С помощью окисления парафина получают кислородосодержащие продукты, в основном органические кислоты. При смешении жидких углеводоpодов с определенным числом атомов углерода получают вазелин, который нашел широкое применение как парфюмерии и косметологии, так и в медицине. Его применяют для приготовления различных мазей, кремов и гелей. А также используют для тепловых процедур в медицине.
Практические задания
1. Запишите общую формулу углеводородов гомологического ряда алканов.
2. Напишите формулы возможных изомеров гексана и назовите их по систематической номенклатуре.
3. Что такое крекинг? Какие виды крекинга вы знаете?
4. Напишите формулы возможных продуктов крекинга гексана.
5. Расшифруйте следующую цепочку превращений. Назовите соединения А, Б и В.
6. Приведите структурную формулу углеводорода С5Н12, образующего при бромировании только одно монобром-производное.
7. На полное сгорание 0,1 моль алкана неизвестного строения израсходовано 11,2 л кислорода (при н. у.). Какова структурная формула алкана?
8. Какова структурная формула газообразного предельного углеводорода, если 11 г этого газа занимают объем 5,6 л (при н. у.)?
9. Вспомните, что вам известно о применении метана, и объясните, почему утечка бытового газа может быть обнаружена по запаху, хотя его составляющие запаха не имеют.
10*. Какие соединения могут быть получены каталитическим окислением метана в различных условиях? Напишите уравнения соответствующих реакций.
11*. Продукты полного сгорания (в избытке кислорода) 10,08 л (н. у.) смеси этана и пропана пропустили через избыток известковой воды. При этом образовалось 120 г осадка. Определите объемный состав исходной смеси.
12*. Плотность по этану смеси двух алканов равна 1,808. При бромировании этой смеси выделено только две пары изомерных монобромалканов. Суммарная масса более легких изомеров в продуктах реакции равна суммарной массе более тяжелых изомеров. Определите объемную долю более тяжелого алкана в исходной смеси.