მაგნიუმი რა ნაწილია. მაგნიუმის იონები ინსულინის ჰემოგლობინის ნაწილია. ძვლოვანი ქსოვილის მინერალურ და ორგანულ კომპონენტებში ასაკთან დაკავშირებული ცვლილებები. როდესაც ორსულს ენიშნება მაგნიუმის პრეპარატები. ურთიერთქმედება სხვა ნივთიერებებთან
მეცნიერება, რომელიც სწავლობს ამ ელემენტებს, არის ქიმია. პერიოდული ცხრილი, რომლის საფუძველზეც შეგვიძლია შევისწავლოთ ეს მეცნიერება, გვიჩვენებს, რომ მაგნიუმის ატომში არის თორმეტი პროტონი და ნეიტრონი. ეს შეიძლება განისაზღვროს ატომური რიცხვით (ეს უდრის პროტონების რაოდენობას და ელექტრონების იგივე რაოდენობა იქნება, თუ ის ნეიტრალური ატომია და არა იონი).
მაგნიუმის ქიმიურ თვისებებს ქიმიაც სწავლობს. პერიოდული ცხრილი ასევე აუცილებელია მათი განსახილველად, რადგან ის გვიჩვენებს ელემენტის ვალენტობას (ამ შემთხვევაში ის უდრის ორს). ეს დამოკიდებულია ჯგუფზე, რომელსაც მიეკუთვნება ატომი. გარდა ამისა, მისი დახმარებით შეგიძლიათ გაიგოთ, რომ მაგნიუმის მოლური მასა ოცდაოთხია. ანუ ამ ლითონის ერთი მოლი იწონის ოცდაოთხ გრამს. მაგნიუმის ფორმულა ძალიან მარტივია - ის არ შედგება მოლეკულებისგან, არამედ ატომებისგან, რომლებიც გაერთიანებულია ბროლის ბადით.
მაგნიუმის მახასიათებლები ფიზიკის თვალსაზრისით
როგორც ყველა ლითონი, გარდა ვერცხლისწყლისა, ამ ნაერთს აქვს აგრეგაციის მყარი მდგომარეობა ნორმალურ პირობებში. მას აქვს ღია ნაცრისფერი ფერი თავისებური ბზინვარებით. ამ ლითონს საკმაოდ მაღალი სიმტკიცე აქვს. მაგნიუმის ფიზიკური მახასიათებლები ამით არ მთავრდება.
განვიხილოთ დნობის და დუღილის წერტილები. პირველი უდრის ექვსას ორმოცდაათი გრადუს ცელსიუსს, მეორე არის ათას ოთხმოცდაათი გრადუსი ცელსიუსი. შეგვიძლია დავასკვნათ, რომ ეს საკმაოდ დნებადი ლითონია. გარდა ამისა, ის ძალიან მსუბუქია: მისი სიმკვრივეა 1,7 გ/სმ3.
მაგნიუმი. ქიმია
იცოდეთ ამ ნივთიერების ფიზიკური მახასიათებლები, შეგიძლიათ გადახვიდეთ მისი მახასიათებლების მეორე ნაწილზე. ამ ლითონს აქვს საშუალო დონის აქტივობა. ეს ჩანს ლითონების ელექტროქიმიური სერიიდან - რაც უფრო პასიურია, მით უფრო მარჯვნივ არის. მაგნიუმი ერთ-ერთი პირველია მარცხნივ. მოდი თანმიმდევრობით განვიხილოთ, რა ნივთიერებებთან რეაგირებს და როგორ ხდება ეს.
მარტივი
ეს მოიცავს მათ, ვისი მოლეკულები შედგება მხოლოდ ერთი ქიმიური ელემენტისგან. ეს მოიცავს ჟანგბადს, ფოსფორს, გოგირდს და ბევრ სხვას. პირველ რიგში, მოდით შევხედოთ ურთიერთქმედებას ჟანგბადთან. წვას ჰქვია. ამ შემთხვევაში წარმოიქმნება ამ ლითონის ოქსიდი. თუ ორ მოლ მაგნიუმს დავწვავთ, ერთი მოლი ჟანგბადის ხარჯვისას მივიღებთ ორ მოლ ოქსიდს. ამ რეაქციის განტოლება დაწერილია შემდეგნაირად: 2Mg + O 2 = 2MgO. გარდა ამისა, როდესაც მაგნიუმი იწვის გარეთიქმნება მისი ნიტრიდიც, ვინაიდან ეს ლითონი ატმოსფეროში შემავალ აზოტთან პარალელურად რეაგირებს.
როდესაც სამი მოლი მაგნიუმი იწვება, ერთი მოლი აზოტი მოიხმარება და შედეგი არის მოცემული ლითონის ერთი მოლი ნიტრიდი. ამ სახის ქიმიური ურთიერთქმედების განტოლება შეიძლება დაიწეროს შემდეგნაირად: 3Mg + N 2 = Mg 3 N 2.

გარდა ამისა, მაგნიუმს შეუძლია რეაგირება სხვა მარტივ ნივთიერებებთან, როგორიცაა ჰალოგენები. მათთან ურთიერთქმედება ხდება მხოლოდ იმ შემთხვევაში, თუ კომპონენტები თბება ძალიან მაღალ ტემპერატურაზე. ამ შემთხვევაში, დამატების რეაქცია ხდება. ჰალოგენებში შედის შემდეგი მარტივი ნივთიერებები: ქლორი, იოდი, ბრომი, ფტორი. და რეაქციებს შესაბამისად ასახელებენ: ქლორირება, იოდირება, ბრომირება, ფტორირება. როგორც თქვენ ალბათ მიხვდით, ასეთი ურთიერთქმედების შედეგად შეიძლება მიიღოთ მაგნიუმის ქლორიდი, იოდიდი, ბრომიდი და ფტორი. მაგალითად, თუ ავიღებთ ერთ მოლ მაგნიუმს და ამდენივე იოდს, მივიღებთ ამ ლითონის ერთ მოლ იოდიდს. ეს ქიმიური რეაქცია შეიძლება გამოიხატოს შემდეგი განტოლების გამოყენებით: Mg + I 2 = MgI 2. ქლორირება ხორციელდება იმავე პრინციპით. აქ არის რეაქციის განტოლება: Mg + Cl 2 = MgCl 2.
გარდა ამისა, ლითონები, მათ შორის მაგნიუმი, რეაგირებენ ფოსფორთან და გოგირდთან. პირველ შემთხვევაში, შეგიძლიათ მიიღოთ ფოსფიდი, მეორეში - სულფიდი (არ აგერიოთ ფოსფატებსა და სულფატებში!). თუ აიღებთ სამ მოლ მაგნიუმს, დაუმატებთ მას ორ მოლ ფოსფორს და გაათბეთ სასურველ ტემპერატურამდე, წარმოიქმნება მოცემული ლითონის ერთი მოლი ფოსფიდი. ამის განტოლება ქიმიური რეაქციაასე გამოიყურება: 3 მგ + 2 პ = მგ 3 პ 2. ანალოგიურად, თუ მაგნიუმს და გოგირდს თანაბარი მოლური პროპორციებით აურიებთ და შექმნით საჭირო პირობებს მაღალი ტემპერატურის სახით, ამ ლითონის სულფიდს ვიღებთ. ასეთი ქიმიური ურთიერთქმედების განტოლება შეიძლება დაიწეროს შემდეგნაირად: Mg + S = MgS. ასე რომ, ჩვენ გადავხედეთ ამ ლითონის რეაქციებს სხვა მარტივ ნივთიერებებთან. მაგრამ ქიმიური დახასიათებამაგნიუმი ამით არ მთავრდება.
რეაქციები რთულ ნაერთებთან
ეს ნივთიერებები მოიცავს წყალს, მარილებს და მჟავებს. ლითონები განსხვავებულად რეაგირებენ სხვადასხვა ჯგუფთან. მოდით შევხედოთ ყველაფერს თანმიმდევრობით.
მაგნიუმი და წყალი
როდესაც ეს ლითონი ურთიერთქმედებს დედამიწაზე ყველაზე გავრცელებულ ქიმიურ ნაერთთან, ოქსიდი და წყალბადი წარმოიქმნება ძლიერი, უსიამოვნო სუნით გაზის სახით. ამ ტიპის რეაქციის განსახორციელებლად საჭიროა კომპონენტების გაცხელებაც. თუ აურიეთ ერთი მოლი მაგნიუმი და წყალი, მიიღებთ იგივე რაოდენობის ოქსიდს და წყალბადს. რეაქციის განტოლება იწერება შემდეგნაირად: Mg + H 2 O = MgO + H 2.
ურთიერთქმედება მჟავებთან
სხვა რეაქტიული ლითონების მსგავსად, მაგნიუმს შეუძლია წყალბადის ატომების გადაადგილება მათი ნაერთებისგან. ამ სახის პროცესს უწოდებენ ასეთ შემთხვევებში, ლითონის ატომები ცვლის წყალბადის ატომებს და წარმოიქმნება მარილი, რომელიც შედგება მაგნიუმის (ან სხვა ელემენტისგან) და მჟავა ნალექისგან. მაგალითად, თუ აიღებთ ერთ მოლ მაგნიუმს და დაუმატებთ ორ მოლს, წარმოიქმნება ერთი მოლი ამ ლითონის ქლორიდი და წყალბადის იგივე რაოდენობა. რეაქციის განტოლება ასე გამოიყურება: Mg + 2HCl = MgCl 2 + H 2.
ურთიერთქმედება მარილებთან
ჩვენ უკვე აღვწერეთ, თუ როგორ წარმოიქმნება მარილები მჟავებისგან, მაგრამ მაგნიუმის დახასიათება ქიმიური თვალსაზრისით ასევე გულისხმობს მარილებთან მისი რეაქციების განხილვას. ამ შემთხვევაში ურთიერთქმედება შეიძლება მოხდეს მხოლოდ იმ შემთხვევაში, თუ მარილში შემავალი ლითონი ნაკლებად აქტიურია ვიდრე მაგნიუმი. მაგალითად, თუ ავიღებთ ერთ მოლ მაგნიუმს და სპილენძის სულფატს, მივიღებთ მოცემული ლითონის სულფატს და სუფთა სპილენძს თანაბარი მოლური თანაფარდობით. ამ ტიპის რეაქციის განტოლება შეიძლება დაიწეროს შემდეგნაირად: Mg + CuSO 4 = MgSO 4 + Cu. სწორედ აქ მოქმედებს მაგნიუმის აღდგენითი თვისებები.

ამ ლითონის გამოყენება
იმის გამო, რომ იგი მრავალი თვალსაზრისით აღემატება ალუმინს - ის დაახლოებით სამჯერ მსუბუქია, მაგრამ ამავე დროს ორჯერ უფრო ძლიერია, იგი ფართოდ გამოიყენება სხვადასხვა ინდუსტრიაში. უპირველეს ყოვლისა, ეს არის თვითმფრინავების ინდუსტრია. აქ მაგნიუმზე დაფუძნებული შენადნობები პოპულარობით პირველ ადგილს იკავებს ყველა გამოყენებულ მასალას შორის. გარდა ამისა, იგი გამოიყენება ქიმიურ მრეწველობაში, როგორც შემცირების აგენტი მათი ნაერთებიდან გარკვეული ლითონების ამოსაღებად. იმის გამო, რომ წვის დროს მაგნიუმი წარმოქმნის ძალიან მძლავრ ციმციმს, იგი გამოიყენება სამხედრო ინდუსტრიაში სიგნალის სროლების, ფლეშ-ხმაურის საბრძოლო მასალის დასამზადებლად და ა.შ.
მაგნიუმის მიღება
ამისათვის მთავარი ნედლეული არის ამ ლითონის ქლორიდი. ეს კეთდება ელექტროლიზით.
ხარისხობრივი რეაქცია მოცემული ლითონის კატიონებზე
ეს არის სპეციალური პროცედურა, რომელიც შექმნილია ნივთიერების იონების არსებობის დასადგენად. ხსნარის შესამოწმებლად მაგნიუმის ნაერთების არსებობისთვის, შეგიძლიათ დაამატოთ კალიუმი ან ნატრიუმის კარბონატი. შედეგად წარმოიქმნება თეთრი ნალექი, რომელიც ადვილად იხსნება მჟავებში.
სად შეიძლება ამ ლითონის პოვნა ბუნებაში?
ეს ქიმიური ელემენტი ბუნებაში საკმაოდ გავრცელებულია. დედამიწის ქერქითითქმის ორი პროცენტი ამ ლითონისგან შედგება. ის გვხვდება ბევრ მინერალში, როგორიცაა კარნალიტი, მაგნეზიტი, დოლომიტი, ტალკი და აზბესტი. პირველი მინერალის ფორმულა ასე გამოიყურება: KCl.MgCl 2 .6H 2 O. ჰგავს მოლურჯო, ღია ვარდისფერი, გაცვეთილი წითელი, ღია ყვითელი ან გამჭვირვალე კრისტალებს.

მაგნეზიტი არის მისი ქიმიური ფორმულა - MgCO 3. ის თეთრი ფერისაა, მაგრამ მინარევებიდან გამომდინარე, შეიძლება ჰქონდეს ნაცრისფერი, ყავისფერი ან ყვითელი ელფერი. დოლომიტს აქვს შემდეგი ქიმიური ფორმულა: MgCO 3 .CaCO 3 . ეს არის მოყვითალო-ნაცრისფერი ან მინერალური შუშის ბზინვარებით.
ტალკს და აზბესტს უფრო რთული ფორმულები აქვთ: 3MgO.4SiO 2 .H 2 O და 3MgO.2SiO 2 .2H 2 O, შესაბამისად. მაღალი სითბოს წინააღმდეგობის გამო, ისინი ფართოდ გამოიყენება ინდუსტრიაში. გარდა ამისა, მაგნიუმი შედის ქიმიური შემადგენლობაუჯრედები და მრავალი ორგანული ნივთიერების სტრუქტურა. ამას უფრო დეტალურად განვიხილავთ.
მაგნიუმის როლი ორგანიზმისთვის
ეს ქიმიური ელემენტი მნიშვნელოვანია როგორც მცენარეული, ასევე ცხოველური არსებებისთვის. მაგნიუმი უბრალოდ სასიცოცხლოდ მნიშვნელოვანია მცენარის ორგანიზმისთვის. როგორც რკინა არის ჰემოგლობინის საფუძველი, რომელიც აუცილებელია ცხოველთა სიცოცხლისთვის, ასევე მაგნიუმი არის ქლოროფილის მთავარი კომპონენტი, რომლის გარეშეც მცენარე ვერ იარსებებს. ეს პიგმენტი ჩართულია ფოტოსინთეზის პროცესში, რომლის დროსაც ხდება საკვები ნივთიერებების სინთეზირება ფოთლებში არსებული არაორგანული ნაერთებისგან.

მაგნიუმი ასევე ძალიან აუცილებელია ცხოველის ორგანიზმისთვის. მასური წილიამ მიკროელემენტის უჯრედში - 0,02-0,03%. იმისდა მიუხედავად, რომ ის ძალიან ცოტაა, ის ასრულებს ძალიან მნიშვნელოვან ფუნქციებს. მისი წყალობით, შენარჩუნებულია ისეთი ორგანელების სტრუქტურა, როგორიცაა მიტოქონდრია, რომლებიც პასუხისმგებელნი არიან უჯრედულ სუნთქვასა და ენერგიის სინთეზზე, ისევე როგორც რიბოზომები, რომლებშიც წარმოიქმნება სიცოცხლისთვის აუცილებელი ცილები. გარდა ამისა, ის არის მრავალი ფერმენტის ქიმიური შემადგენლობის ნაწილი, რომლებიც საჭიროა უჯრედშიდა მეტაბოლიზმისა და დნმ-ის სინთეზისთვის.
მთლიანობაში ორგანიზმისთვის, მაგნიუმი აუცილებელია გლუკოზის, ცხიმების და ზოგიერთი ამინომჟავის მეტაბოლიზმში მონაწილეობის მისაღებად. ასევე, ამ მიკროელემენტის დახმარებით შესაძლებელია ნერვული სიგნალის გადაცემა. ყოველივე ზემოთქმულის გარდა, ორგანიზმში საკმარისი მაგნიუმი ამცირებს ინფარქტის, ინფარქტის და ინსულტის რისკს.
გაზრდილი და შემცირებული შემცველობის სიმპტომები ადამიანის ორგანიზმში
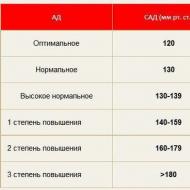
ორგანიზმში მაგნიუმის ნაკლებობა ვლინდება ისეთი ძირითადი სიმპტომებით, როგორიცაა მაღალი წნევა, დაღლილობა და დაბალი შრომისუნარიანობა, გაღიზიანება და ცუდი სიზმარი, მეხსიერების დაქვეითება, ხშირი თავბრუსხვევა. ასევე შეიძლება განიცადოთ გულისრევა, კრუნჩხვები, თითების კანკალი, დაბნეულობა - ეს არის საკვებიდან ამ მიკროელემენტის ძალიან დაბალი დონის ნიშნები.

ორგანიზმში მაგნიუმის ნაკლებობა იწვევს ხშირ რესპირატორულ დაავადებებსა და მუშაობის დარღვევას გულ-სისხლძარღვთა სისტემაასევე ტიპი 2 დიაბეტი. შემდეგი, მოდით შევხედოთ პროდუქტებში მაგნიუმის შემცველობას. მისი დეფიციტის თავიდან ასაცილებლად, თქვენ უნდა იცოდეთ რომელი საკვებია მდიდარი ამ ქიმიური ელემენტით. გასათვალისწინებელია ისიც, რომ ამ სიმპტომთაგან ბევრი შეიძლება გამოვლინდეს საპირისპირო შემთხვევაშიც - ორგანიზმში მაგნიუმის ჭარბი რაოდენობით, ასევე ისეთი მიკროელემენტების ნაკლებობით, როგორიცაა კალიუმი და ნატრიუმი. ამიტომ, მნიშვნელოვანია, ყურადღებით გადახედოთ თქვენს დიეტას და გაიგოთ პრობლემის არსი, ეს საუკეთესოდ კეთდება დიეტოლოგის დახმარებით.
როგორც ზემოთ აღინიშნა, ეს ელემენტი არის ქლოროფილის მთავარი კომპონენტი. აქედან გამომდინარე, შეგიძლიათ გამოიცნოთ, რომ მას დიდი რაოდენობით შეიცავს მწვანილი: ნიახური, კამა, ოხრახუში, ყვავილოვანი კომბოსტო და თეთრი კომბოსტო, სალათის ფოთოლი და ა.შ. ასევე ბევრი მარცვლეული, განსაკუთრებით წიწიბურა და ფეტვი, ასევე შვრიის ფაფა და ქერი. გარდა ამისა, თხილი მდიდარია ამ მიკროელემენტით: კეშიუ და კაკალი, და არაქისი, და თხილი და ნუში. პარკოსნები, როგორიცაა ლობიო და ბარდა, ასევე შეიცავს დიდი რაოდენობით ამ ლითონს.

ბევრი ის ასევე გვხვდება წყალმცენარეებში, მაგალითად ზღვის მცენარეები. თუ ამ პროდუქტებს მოიხმარენ ნორმალური რაოდენობით, მაშინ თქვენს ორგანიზმს არ დააკლდება ამ სტატიაში განხილული ლითონი. თუ არ გაქვთ საშუალება რეგულარულად მიირთვათ ზემოთ ჩამოთვლილი საკვები, უმჯობესია შეიძინოთ ამ მიკროელემენტის შემცველი საკვები დანამატები. თუმცა, სანამ ამას გააკეთებთ, აუცილებლად უნდა მიმართოთ ექიმს.
დასკვნა
მაგნიუმი მსოფლიოში ერთ-ერთი ყველაზე მნიშვნელოვანი ლითონია. მან იპოვა ფართო გამოყენება მრავალ ინდუსტრიაში - ქიმიურიდან საავიაციო და სამხედრო. უფრო მეტიც, ეს ძალიან მნიშვნელოვანია ბიოლოგიური თვალსაზრისით. მის გარეშე შეუძლებელია არც მცენარეული და არც ცხოველური ორგანიზმების არსებობა. ამის წყალობით ქიმიური ელემენტი, მიმდინარეობს პროცესი, რომელიც სიცოცხლეს აძლევს მთელ პლანეტას - ფოტოსინთეზი.
- გავლენა სხეულის ძირითად ფუნქციებზე: ფერმენტების გააქტიურება, ცილის სინთეზი, გულის არტერიის ჯანმრთელობა, ნერვის ფუნქცია.
- ამ მინერალის მინიმალური დღიური მოთხოვნილება (RDA) და საუკეთესო საკვები წყაროები: 150 მგ - მარცვლეულის ფაფები, სპეციალური თევზის კერძები, მწვანე მცენარეების ფოთლები.
- სინერგიზმი საკვები დანამატებთან და სხვა ვიტამინებთან და მინერალებთან (სხეულზე ზემოქმედების გაუმჯობესება და გაძლიერება): B 6, C, კალციუმი, ფოსფორი.
- დეფიციტის სიმპტომები: ზრდის ნაკლებობა, ფეხის კრუნჩხვები, ნერვიულობა.
- ფაქტორები, რომლებიც ამცირებს ამ მინერალის დონეს ორგანიზმში: ჭარბი რკინა.
- ქიმიური მახასიათებლები:
- სერია N - 12
- ატომური წონა - 24,32
გაცხელებისას ადვილად იწვის, გადაიქცევა ოქსიდ - MgO - დამწვრობის მაგნეზიაში. ამ შემთხვევაში, მაგნიუმის ციმციმი ხდება. ადვილად ერწყმის ჰალოიდებს, ხოლო გაცხელებისას - გოგირდთან და აზოტთან.
მაგნიუმის ოქსიდი არის თეთრი ფხვნილი, ადვილად ხსნადი მჟავებში; წყალთან ერთად მაგნიუმის ოქსიდი წარმოქმნის ჰიდრატს - Mg(OH) 2, რომელიც წარმოადგენს საშუალო სიძლიერის ფუძეს.
მაგნიუმის მარილების უმეტესობა წყალში ძალიან ხსნადია.
მაგნიუმის იონების არსებობა სითხეს მწარე გემოს აძლევს.NB!ჯგუფში მაგნიუმის უახლოესი მეზობელია კალციუმი, რომელთანაც მაგნიუმი შედის გაცვლით რეაქციებში. ეს ორი ელემენტი ადვილად აშორებს ერთმანეთს მათი კავშირებიდან.
- ზოგადი ინფორმაცია:
მაგნიუმი ბუნებაში ერთ-ერთი ყველაზე გავრცელებული ელემენტია. განსაკუთრებით ბევრია მაგნიუმის ქლორიდი ზღვის წყალი. სასმელი წყალი ასევე შეიცავს მაგნიუმის იონებს.
IN ფლორამაგნიუმი მნიშვნელოვან როლს ასრულებს ქლოროფილის შემადგენლობაში. მაგნიუმის გარეშე არ შეიძლება იყოს არც მწვანე მცენარეები და არც ცხოველები, რომლებიც მათზე იკვებებიან. - ფიზიოლოგია:
მაგნიუმი ორგანიზმში შედის საკვებით, წყლით და მარილით. მაგნიუმით განსაკუთრებით მდიდარია მცენარეული საკვები. იონიზებული მაგნიუმის ნაწილი გამოიყოფა კუჭში არსებული საკვების მაგნიუმის მარილებისგან და შეიწოვება სისხლში. მცირედ ხსნადი მაგნიუმის მარილების ძირითადი ნაწილი გადადის ნაწლავებში და მხოლოდ ცხიმოვან და ტუტე მჟავებთან შერწყმის შემდეგშეიწოვება სისხლში. მაგნიუმის კომპლექსური ნაერთები გადადის ღვიძლში. ორგანოებში მათი შემდგომი გავრცელების გზები ჯერ არ არის შესწავლილი.
მაგნიუმის მთავარი "საწყობი".გვხვდება ძვლებში და კუნთებში. ძვლები შეიცავს მაგნიუმის ფოსფატს 1,5%, კბილების მინანქარი შეიცავს 0,75% (კარიესულ კბილებში 0,83-1,88%).მაგნიუმის კონცენტრაცია ადამიანის სისხლში არის 2,3-4,0 მგ%.
ყოველდღიური საჭიროებამაგნიუმში - 0,6 მგ.
ნორმალური მაგნიუმი გამოირჩევათირკმელებით ფოსფატების სახით, მაგრამ ძირითადად ნაწლავებით 0,2-0,3 მგ/დღეში. - მნიშვნელობა:
მაგნიუმი აუცილებელია განუყოფელი ნაწილიყველა უჯრედი და ქსოვილი, რომელიც თავის ადგილზე მონაწილეობს სხვა ელემენტების იონებთან ერთად იონური ბალანსის შენარჩუნებასხეულის სითხეები.
მაგნიუმი არის ფერმენტების ნაწილი, რომლებიც დაკავშირებულია ფოსფორისა და ნახშირწყლების მეტაბოლიზმთან. მაგნიუმი ააქტიურებს პლაზმასა და ძვლის ფოსფატაზას და მონაწილეობს ნეირომუსკულური აგზნებადობის პროცესში. - ჭარბი მაგნიუმი და მისი გამოვლინებები:
მაგნიუმის მარილების დიდ დოზებს ძირითადად აქვს დამამშვიდებელი ეფექტი (განსაკუთრებით მაგნიუმის სულფატი).
მაგნიუმის სულფატის პარენტერალურად მიღებისას აღინიშნება სიმპტომები: ზოგადი დეპრესია, ლეთარგია, ძილიანობა, ანესთეზია ხდება მაგნიუმის კონცენტრაციით 15-18 მგ%-მდე (ნორმის ნაცვლად - 4 მგ%).
მაგნიუმის მარილების ანესთეზიის გამოწვევის უნარი პირველად აღმოაჩინეს მელცერმა და აუერმა 1905 წელს.
ამ ფენომენის უფრო დეტალურმა შესწავლამ აჩვენა, რომ 25% MgSO 4 ხსნარი, რომელიც შეყვანილია ინტრადურალურ სივრცეში, მოქმედებს როგორც კოკაინი, რაც იწვევს სრულ ანესთეზიას. - მაგნიუმის დეფიციტი და მისი გამოვლინებები:
როდესაც სისხლში მაგნიუმის კონცენტრაცია ნორმალურ ზღვარს ქვემოთ (2,3-4,0 მგ) იკლებს, ვლინდება აგზნების სიმპტომები. ნერვული სისტემებიკრუნჩხვამდე.
ჩვილების სისხლში მაგნიუმის დაქვეითებამ (განსაკუთრებით ხელოვნური კვების დროს) შეიძლება გამოიწვიოს ტეტანია. ეს აიხსნება იმით, რომ მიუხედავად იმისა, რომ მაგნიუმის შემცველობა ძროხის რძეში 4-ჯერ მეტია, ვიდრე ქალის რძეში, ძროხის რძისგან მიღებული მაგნიუმი გაცილებით რთულია.
ბავშვებში მაგნიუმის სისხლში დაქვეითება შეინიშნება რაქიტის დროსაც და ამ შემთხვევაში რაქიტის ბავშვებში მაგნიუმის შეყვანა ხელს უწყობს ორგანიზმში Ca:P თანაფარდობის გაუმჯობესებას.
კალციუმით მდიდარი რაციონიდან მაგნიუმის გამორიცხვა იწვევს კალციუმის შეკავებას ყველა ქსოვილში, განსაკუთრებით გულის კუნთსა და თირკმელებში, რაც იწვევს მათ კალციფიკაციას.
მაგნიუმი ბუნებაში ფართოდ გავრცელებული და ადამიანისთვის დიდი ბიოგენური მნიშვნელობის ლითონია. ეს არის დიდი რაოდენობით სხვადასხვა მინერალების, ზღვის წყლის და ჰიდროთერმული წყლების კომპონენტი.
თვისებები
ვერცხლისფერი მბზინავი ლითონი, ძალიან მსუბუქი და დრეკადი. არამაგნიტური, აქვს მაღალი თბოგამტარობა. ჰაერში ნორმალურ პირობებში იგი დაფარულია ოქსიდის ფირით. 600 °C-ზე ზევით გაცხელებისას ლითონი იწვის, გამოყოფს დიდი რაოდენობით სითბოს და შუქს. იწვის ნახშირორჟანგიდა აქტიურად რეაგირებს წყალთან, ამიტომ მისი ჩაქრობა ტრადიციული მეთოდებით აზრი არ აქვს.
მაგნიუმი არ ურთიერთქმედებს ტუტეებთან, ის რეაგირებს მჟავებთან წყალბადის გამოყოფის მიზნით. მდგრადია ჰალოგენებისა და მათი ნაერთების მიმართ; მაგალითად, არ ურთიერთქმედებს ფტორთან, ჰიდროფლუორმჟავასთან, მშრალ ქლორთან, იოდთან, ბრომთან. ის არ ნადგურდება ნავთობპროდუქტების გავლენის ქვეშ. მაგნიუმი ცუდად მდგრადია კოროზიის მიმართ.
მაგნიუმი აუცილებელია გულ-სისხლძარღვთა და ნერვული სისტემების ჯანმრთელობისთვის, ცილების სინთეზისთვის და ორგანიზმის მიერ გლუკოზის, ცხიმებისა და ამინომჟავების ათვისებისთვის. მაგნიუმის ოროტატი (ვიტამინი B13) მნიშვნელოვან როლს ასრულებს მეტაბოლიზმში, ახდენს გულის აქტივობის ნორმალიზებას, ხელს უშლის ქოლესტერინის დეპონირებას სისხლძარღვების კედლებზე, ზრდის სპორტსმენების მუშაობას, არის ისეთივე ეფექტური, როგორც სტეროიდული პრეპარატები.
მიიღეთ მაგნიუმი სხვადასხვა გზით, დან ბუნებრივი მინერალებიდა ზღვის წყალი.
 განაცხადი
განაცხადი
მოპოვებული მაგნიუმის უმეტესი ნაწილი გამოიყენება მაგნიუმის სტრუქტურული შენადნობების წარმოებისთვის, რომლებიც მოთხოვნადია საავიაციო, საავტომობილო, ბირთვული, ქიმიური, ნავთობგადამამუშავებელი მრეწველობისა და ხელსაწყოების წარმოებაში. მაგნიუმის შენადნობები გამოირჩევა სიმსუბუქით, სიმტკიცით, მაღალი სპეციფიკური სიმკვეთრით და კარგი დამუშავებით. ისინი არ არიან მაგნიტური, შესანიშნავი სითბოს გაფრქვევა და 20-ჯერ უფრო მდგრადია ვიბრაციის მიმართ, ვიდრე შენადნობი ფოლადი. მაგნიუმის შენადნობები გამოიყენება ბენზინისა და ნავთობპროდუქტების შესანახი ავზების, ბირთვული რეაქტორების ნაწილების, ჩაქუჩების, პნევმატური მილების, მანქანების შესანახად; ავზები და ტუმბოები ფტორმჟავასთან მუშაობისთვის, ბრომისა და იოდის შესანახად; ლეპტოპის და კამერის ქეისები.
- მაგნიუმი ფართოდ გამოიყენება შემცირებით ზოგიერთი ლითონის მისაღებად (ვანადიუმი, ცირკონიუმი, ტიტანი, ბერილიუმი, ქრომი და სხვ.); ფოლადისა და თუჯის უკეთესი მექანიკური მახასიათებლების მისაცემად, ალუმინის გასაწმენდად.
- მისი სუფთა სახით, ის მრავალი ნახევარგამტარის ნაწილია.
- ქიმიურ მრეწველობაში ფხვნილ მაგნიუმს იყენებენ ორგანული ნივთიერებების გასაშრობად, მაგალითად, ალკოჰოლის, ანილინის. მაგნიუმი ორგანული ნაერთებიგამოიყენება კომპლექსურ ქიმიურ სინთეზში (მაგალითად, A ვიტამინის მისაღებად).
- მაგნიუმის ფხვნილი მოთხოვნადია სარაკეტო ტექნოლოგიაში, როგორც მაღალკალორიული საწვავი. სამხედრო საქმეებში - ცეცხლსასროლი იარაღის, მკვლევარის საბრძოლო მასალის, ცეცხლგამჩენი ბომბების წარმოებაში.
- სუფთა მაგნიუმი და მისი ნაერთები გამოიყენება ძლიერი ქიმიური დენის წყაროების შესაქმნელად.
- მაგნიუმის ოქსიდი გამოიყენება ჭურჭლისა და მეტალურგიული ღუმელების დასამზადებლად, ცეცხლოვანი აგური, სინთეზური რეზინის წარმოებაში.
- ოპტიკაში მოთხოვნადია მაგნიუმის ფტორიდის კრისტალები. 
- მაგნიუმის ჰიდრიდი არის მყარი ფხვნილი, რომელიც შეიცავს წყალბადის მაღალ პროცენტს, რომელიც ადვილად მიიღება გაცხელებით. ნივთიერება გამოიყენება წყალბადის "საწყობად".
- ახლა ნაკლებად გავრცელებულია, მაგრამ ადრე მაგნიუმის ფხვნილი ფართოდ გამოიყენებოდა ქიმიურ ციმციმებში.
- მაგნიუმის ნაერთები გამოიყენება ქსოვილების გასათეთრებლად და ატრასისთვის, თბოსაიზოლაციო მასალების და სპეციალური ტიპის აგურის დასამზადებლად.
- მაგნიუმი ბევრის ნაწილია წამლები, როგორც შიდა, ასევე გარე (ბიშოფიტი) გამოყენება. გამოიყენება როგორც კრუნჩხვის საწინააღმდეგო, საფაღარათო, დამამშვიდებელი, გულის, სპაზმის საწინააღმდეგო საშუალება, კუჭის წვენის მჟავიანობის დასარეგულირებლად, მჟავით მოწამვლის საწინააღმდეგოდ, კუჭის სადეზინფექციო საშუალებად, დაზიანებებისა და სახსრების სამკურნალოდ.
- მაგნიუმის სტეარატი გამოიყენება ფარმაცევტულ და კოსმეტიკურ ინდუსტრიაში, როგორც შემავსებელი ტაბლეტებში, ფხვნილებში, კრემებში, თვალის ჩრდილებში; ვ კვების მრეწველობაგამოიყენება როგორც საკვები დანამატი E470, რომელიც ხელს უშლის პროდუქტების შეკუმშვას.
Prime Chemicals Group-ის ქიმიურ მაღაზიაში შეგიძლიათ შეიძინოთ ქიმიური მაგნიუმი და მისი სხვადასხვა კავშირები- მაგნიუმის სტეარატი, ბიშოფიტი მაგნიუმის ქლორიდი, მაგნიუმის კარბონატი და სხვა, აგრეთვე ქიმიური რეაგენტების ფართო სპექტრი, ლაბორატორიული მინის ჭურჭელი და სხვა საქონელი ლაბორატორიებისა და წარმოებისთვის. მოგეწონებათ ფასები და მომსახურების დონე!
ეს არის ბუნებრივი დამამშვიდებელი და სტრესის საწინააღმდეგო მინერალი!
მაგნიუმი ბუნებაში ერთ-ერთი ყველაზე გავრცელებული ელემენტია, ის არის ადამიანისა და ცხოველის ძვლებისა და კბილის მინანქრის განუყოფელი კომპონენტი და მცენარეებში ქლოროფილის ნაწილია. მაგნიუმის იონები გვხვდება სასმელი წყალიდა ზღვის წყალი შეიცავს უამრავ მაგნიუმის ქლორიდს.
ორგანიზმი შეიცავს 20-30 გ მაგნიუმს. მაგნიუმის დაახლოებით 1% გვხვდება სხეულის სითხეებში, ხოლო დარჩენილი 99% გვხვდება ძვლებში (დაახლოებით 40%) და რბილ ქსოვილებში (დაახლოებით 59%).
მაგნიუმით მდიდარი საკვები
მითითებულია სავარაუდო ხელმისაწვდომობა 100 გ პროდუქტში
მაგნიუმის ყოველდღიური მოთხოვნილებაა 400-500 მგ.
მაგნიუმის საჭიროება იზრდება:
- სტრესი;
- დიეტაში დიდი რაოდენობით ცილის შემცველობა;
- ახალი ქსოვილების სწრაფი ფორმირება - ბავშვებში, ბოდიბილდერებში;
- ორსულობა და ძუძუთი კვება;
- დიურეზულების მიღება.
მონელება
მაგნიუმი შეიწოვება ძირითადად თორმეტგოჯა ნაწლავში და ოდნავ მსხვილ ნაწლავში. მაგრამ მხოლოდ ორგანული მაგნიუმის ნაერთები კარგად შეიწოვება, მაგალითად, ორგანული მაგნიუმის ნაერთები კომპლექსებში ამინომჟავებთან, ორგანულ მჟავებთან (მაგნიუმის ლაქტატი, მაგნიუმის ციტრატი) და ა.შ. არაორგანული მარილები (მაგნიუმის სულფატი) ძალიან ცუდად შეიწოვება.
კალციუმის (Ca), ფოსფორის (P), ნატრიუმის (Na) და ცხიმების გადაჭარბებული მიღება აფერხებს მაგნიუმის შეწოვას. დიეტური ბოჭკოვანი აკავშირებს მაგნიუმს, ხოლო ჭარბი ალკოჰოლი, კოფეინი და კალიუმი (K) ზრდის შარდში მაგნიუმის დაკარგვას.
მაგნიუმის სასარგებლო თვისებები და მისი გავლენა სხეულზე
მაგნიუმი მნიშვნელოვან როლს ასრულებს ორგანიზმში - ის აუცილებელია 300-მდე ფერმენტის ნორმალური ფუნქციონირებისთვის. კალციუმთან (Ca) და ფოსფორთან (P) ერთად მაგნიუმი მონაწილეობს ჯანსაღი ძვლების ფორმირებაში.
მაგნიუმი აუცილებელია გლუკოზის, ამინომჟავების, ცხიმების მეტაბოლიზმისთვის, საკვები ნივთიერებების ტრანსპორტირებისთვის და საჭიროა ენერგიის წარმოებისთვის. მაგნიუმი მონაწილეობს ცილის სინთეზის, გენეტიკური ინფორმაციის გადაცემის და ნერვული სიგნალების პროცესში. აუცილებელია ჯანსაღი გულ-სისხლძარღვთა სისტემის შესანარჩუნებლად. მაგნიუმის ადეკვატური დონე ამცირებს გულის შეტევის ალბათობას.
მაგნიუმი ახდენს კუნთების აქტივობის ნორმალიზებას, ამცირებს ქოლესტერინს და ეხმარება ორგანიზმის გაწმენდას გარკვეული ტიპის ტოქსიკური ნივთიერებებისგან.
მაგნიუმი ვიტამინ B6-თან ერთად (პირიდოქსინი) ხელს უშლის თირკმლის ქვების წარმოქმნას. თუ მხოლოდ მაგნიუმი აკლია, თირკმლის ქვები ყველაზე ხშირად ფოსფატური ქვებია (კალციუმის ნაერთები ფოსფორთან ერთად), ხოლო თუ მხოლოდ ვიტამინი B6 აკლია, ჩნდება ოქსალატური ქვები (კალციუმის (Ca) ნაერთები ოქსილის მჟავასთან ერთად).
ის ცნობილია როგორც სტრესის საწინააღმდეგო ნივთიერება- დამატებითი მაგნიუმი ხელს უწყობს სტრესისადმი წინააღმდეგობის გაზრდას. მაგნიუმის მარილები აფერხებენ ავთვისებიანი სიმსივნეების ზრდას.
მაგნიუმი ასევე ეხმარება დაღლილობასთან ბრძოლაში – ქრონიკული დაღლილობის დროს რეკომენდებულია მაგნიუმის შემცველი დანამატების გამოყენება.
ურთიერთქმედება სხვა არსებით ელემენტებთან
მაგნიუმი ნატრიუმთან (Na) და ფოსფორთან (P) ერთად მონაწილეობს სხეულის კუნთოვან და ნერვულ აქტივობაში. ვიტამინი D არეგულირებს მაგნიუმის მეტაბოლიზმს, რითაც ზრდის მისი მოქმედების ეფექტურობას. ვიტამინი E, ვიტამინი B6 და კალიუმი (K) ასევე აუმჯობესებს მაგნიუმის მეტაბოლიზმს. მაგნიუმის ნაკლებობით, კალიუმი (K) არ ინახება უჯრედებში.
ადამიანის ორგანიზმში კალციუმი და მაგნიუმი ერთმანეთთან გარკვეულ თანაფარდობაში უნდა იყოს.
ითვლება, რომ ეს თანაფარდობა არ უნდა იყოს 1:0.6-ზე მეტი. ამრიგად, მაგნიუმის დეფიციტით, კალციუმი იკარგება შარდში, ხოლო ჭარბი კალციუმი, თავის მხრივ, იწვევს მაგნიუმის დეფიციტს.
მაგნიუმის დეფიციტი და ჭარბი რაოდენობა
- მაგნიუმის დეფიციტის ნიშნები
- უძილობა, დილის დაღლილობა (ხანგრძლივი ძილის შემდეგაც კი);
- გაღიზიანება, ხმაურისადმი მომატებული მგრძნობელობა, უკმაყოფილება;
- თავბრუსხვევა, წონასწორობის დაკარგვა;
- თვალების წინ მბჟუტავი წერტილების გამოჩენა;
- არტერიული წნევის ცვლილებები, არარეგულარული გულისცემა;
- კუნთების სპაზმი, კრუნჩხვები, კრუნჩხვები;
- სპაზმური ტკივილი კუჭში, რომელსაც თან ახლავს დიარეა;
- თმის ცვენა, მტვრევადი ფრჩხილები;
ხშირი თავის ტკივილი.
- ჭარბი მაგნიუმის ნიშნები
- ძილიანობა, კოორდინაციის დაკარგვა, მეტყველება;
- ლეთარგია;
- ნელი გულისცემა;
- გულისრევა, ღებინება, დიარეა;
მშრალი ლორწოვანი გარსები (განსაკუთრებით პირის ღრუ). TOგაზრდილი შინაარსი
სისხლში მაგნიუმი (ჰიპერმაგნიემია) გამოწვეულია მაგნიუმის დანამატების გადაჭარბებული მიღებით, კალციუმის (Ca) დანამატებით კომპენსაციის გარეშე.
ფაქტორები, რომლებიც გავლენას ახდენენ საკვებში მაგნიუმის შემცველობაზეთანამედროვე მეთოდები დამუშავებაკვების პროდუქტები