
ალკანები - ნომენკლატურა, მომზადება, ქიმიური თვისებები. ალკანები სინოფსისი ალკანების ქიმიური თვისებები და მიღების მეთოდები
ალკანების აგებულება
ალკანები არის ნახშირწყალბადები, რომელთა მოლეკულებში ატომები დაკავშირებულია ცალკეული ბმებით და რომლებიც შეესაბამება ზოგად ფორმულას. C n H 2n+2. ალკანის მოლეკულებში ნახშირბადის ყველა ატომი მდგომარეობაშია sp 3 ჰიბრიდიზაცია.
ეს ნიშნავს, რომ ნახშირბადის ატომის ოთხივე ჰიბრიდული ორბიტალი ფორმაში, ენერგიით ერთნაირია და მიმართულია ტოლგვერდა კუთხეებისკენ. სამკუთხა პირამიდა - ტეტრაედონი. ორბიტალებს შორის კუთხეებია 109° 28'. თითქმის თავისუფალი ბრუნვა შესაძლებელია ერთი ნახშირბად-ნახშირბადის ბმის ირგვლივ და ალკანის მოლეკულებს შეუძლიათ მიიღონ მრავალფეროვანი ფორმები ნახშირბადის ატომების კუთხეებით ტეტრაედასთან ახლოს (109° 28'), მაგალითად, n-პენტანის მოლეკულაში.

განსაკუთრებით ღირს ალკანების მოლეკულებში არსებული ბმების გახსენება. გაჯერებული ნახშირწყალბადების მოლეკულებში ყველა ბმა ერთია. გადახურვა ხდება ატომების ბირთვების დამაკავშირებელი ღერძის გასწვრივ, ანუ ეს σ-ბმები. ნახშირბად-ნახშირბადის ბმები არაპოლარული და ცუდად პოლარიზებადია. სიგრძე C-C კავშირიალკანებში არის 0,154 ნმ (1,54 10 10 მ). C-H ობლიგაციები გარკვეულწილად მოკლეა. ელექტრონის სიმკვრივე ოდნავ გადადის უფრო ელექტროუარყოფითი ნახშირბადის ატომისკენ, ანუ C-H ბმა არის სუსტად პოლარული.
მეთანის ჰომოლოგიური სერია
ჰომოლოგებინივთიერებები, რომლებიც მსგავსია სტრუქტურით და თვისებებით, მაგრამ განსხვავდებიან ერთმანეთისაგან ერთი ან მეტი CH ჯგუფი 2 .


შეზღუდეთ ნახშირწყალბადებიშეადგენენ მეთანის ჰომოლოგიურ სერიას.
ალკანების იზომერიზმი და ნომენკლატურა
ალკანებს ახასიათებთ ე.წ სტრუქტურული იზომერიზმი. სტრუქტურული იზომერები ერთმანეთისგან განსხვავდებიან ნახშირბადის ჩონჩხის აგებულებით. უმარტივესი ალკანი, რომელიც ხასიათდება სტრუქტურული იზომერებით, არის ბუტანი.
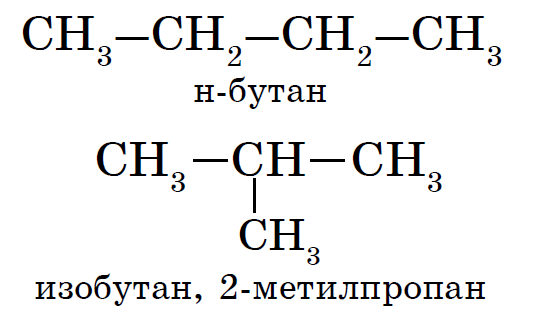
ალკანებისთვის უფრო დეტალურად განვიხილოთ ნომენკლატურის საფუძვლები IUPAC.
1. მთავარი მიკროსქემის შერჩევა. ნახშირწყალბადის სახელის ფორმირება იწყება მთავარი ჯაჭვის განსაზღვრით - ნახშირბადის ატომების ყველაზე გრძელი ჯაჭვი მოლეკულაში, რაც, როგორც იქნა, მისი საფუძველია.
2. ძირითადი ჯაჭვის ატომური ნუმერაცია. მთავარი ჯაჭვის ატომებს ენიჭებათ რიცხვები. ძირითადი ჯაჭვის ატომების ნუმერაცია იწყება შემცვლელთან ყველაზე ახლოს ბოლოდან (სტრუქტურები A, B). თუ შემცვლელები ჯაჭვის ბოლოდან თანაბარ მანძილზე არიან, მაშინ ნუმერაცია იწყება ბოლოდან, სადაც მეტია (სტრუქტურა B). თუ სხვადასხვა შემცვლელი ჯაჭვის ბოლოებიდან თანაბარ მანძილზეა, მაშინ ნუმერაცია იწყება იმ ბოლოდან, რომელთანაც უფრო ძველია (სტრუქტურა G). ნახშირწყალბადების შემცვლელების ასაკი განისაზღვრება თანმიმდევრობით, რომლითაც იწყება მათი სახელი ანბანში: მეთილი (-CH 3), შემდეგ პროპილი (-CH 2 -CH 2 -CH 3), ეთილი (-CH 2 -CH 3) და ა.შ.
გაითვალისწინეთ, რომ შემცვლელის სახელი იქმნება შესაბამისი ალკანის სახელში -an სუფიქსის -yl-ით ჩანაცვლებით.
3. სახელის ფორმირება. სახელის დასაწყისში მითითებულია რიცხვები - ნახშირბადის ატომების რიცხვები, რომლებზეც განლაგებულია შემცვლელები. თუ მოცემულ ატომზე არის რამდენიმე შემცვლელი, მაშინ სახელში შესაბამისი რიცხვი მეორდება ორჯერ მძიმით გამოყოფილი (2,2-). ნომრის შემდეგ დეფისი მიუთითებს შემცვლელების რაოდენობას (დი - ორი, სამი - სამი, ტეტრა - ოთხი, პენტა - ხუთი) და შემცვლელის სახელს (მეთილი, ეთილი, პროპილი). შემდეგ სივრცეებისა და დეფისების გარეშე - მთავარი ჯაჭვის სახელი. მთავარ ჯაჭვს უწოდებენ ნახშირწყალბადს - მეთანის ჰომოლოგიური სერიის წევრი (მეთანი, ეთანი, პროპანი და სხვ.).




იმ ნივთიერებების სახელები, რომელთა სტრუქტურული ფორმულები მოცემულია ზემოთ, შემდეგია:
სტრუქტურა A: 2-მეთილპროპანი;
სტრუქტურა B: 3-ეთილჰექსანი;
სტრუქტურა B: 2,2,4-ტრიმეთილპენტანი;
სტრუქტურა D: 2-მეთილ 4-ეთილჰექსანი.
მოლეკულებში გაჯერებული ნახშირწყალბადების არარსებობა პოლარული ობლიგაციებიმივყავართ მათ წყალში ცუდად ხსნადი, არ ურთიერთქმედებენ დამუხტულ ნაწილაკებთან (იონებთან). ალკანებისთვის ყველაზე ტიპიური რეაქციებია ჩართული რეაქციები თავისუფალი რადიკალები.
ალკანების ფიზიკური თვისებები
მეთანის ჰომოლოგიური სერიის პირველი ოთხი წარმომადგენელი - გაზები. მათგან უმარტივესი არის მეთანი - უფერო, უგემოვნო და უსუნო გაზი („გაზის“ სუნი, რომელსაც იგრძნობთ, რომელიც უნდა დარეკოთ 04-ზე, განისაზღვრება მერკაპტანების სუნით - გოგირდის შემცველი ნაერთები, რომლებიც სპეციალურად ემატება მეთანს, რომელიც გამოიყენება მეთანში. საყოფაცხოვრებო და სამრეწველო გაზის მოწყობილობები, რათა მათ ახლოს მყოფ ადამიანებს შეეძლოთ გაჟონვის სუნი).
ნახშირწყალბადების შემადგენლობა FROM 5 ჰ 12 ადრე FROM 15 ჰ 32 - სითხეები; მძიმე ნახშირწყალბადები არის მყარი. ალკანების დუღილის და დნობის წერტილები თანდათან იზრდება ნახშირბადის ჯაჭვის სიგრძის მატებასთან ერთად. ყველა ნახშირწყალბადები ცუდად ხსნადია წყალში; თხევადი ნახშირწყალბადები ჩვეულებრივი ორგანული გამხსნელებია.


ალკანების ქიმიური თვისებები
ჩანაცვლების რეაქციები.
ალკანებისთვის ყველაზე დამახასიათებელი რეაქციებია რეაქციები თავისუფალი რადიკალების ჩანაცვლება, რომლის დროსაც წყალბადის ატომი იცვლება ჰალოგენის ატომით ან რომელიმე ჯგუფით.
წარმოგიდგენთ მახასიათებლის განტოლებებს ჰალოგენაციის რეაქციები:
ჰალოგენის სიჭარბის შემთხვევაში, ქლორირება შეიძლება უფრო შორს წავიდეს, წყალბადის ყველა ატომის ქლორით სრულ ჩანაცვლებამდე:

მიღებული ნივთიერებები ფართოდ გამოიყენება როგორც გამხსნელები და საწყისი მასალები ორგანულ სინთეზში.
დეჰიდროგენაციის რეაქცია(წყალბადის გაყოფა).
ალკანების კატალიზატორზე (Pt, Ni, Al 2 O 3, Cr 2 O 3) გავლის დროს მაღალ ტემპერატურაზე (400-600 ° C), წყალბადის მოლეკულა იყოფა და წარმოიქმნება ალკენი:
რეაქციები, რომელსაც თან ახლავს ნახშირბადის ჯაჭვის განადგურება. ყველა გაჯერებული ნახშირწყალბადები იწვიანნახშირორჟანგის და წყლის წარმოქმნით. აირისებრი ნახშირწყალბადები, რომლებიც შერეულია ჰაერთან გარკვეული პროპორციებით, შეიძლება აფეთქდეს.
1. გაჯერებული ნახშირწყალბადების წვაარის თავისუფალი რადიკალების ეგზოთერმული რეაქცია, რომელსაც აქვს ძალიან დიდი მნიშვნელობაალკანების საწვავად გამოყენებისას:
ზოგადად, ალკანების წვის რეაქცია შეიძლება დაიწეროს შემდეგნაირად:
2. ნახშირწყალბადების თერმული დაშლა.
პროცესი გრძელდება თავისუფალი რადიკალების მექანიზმი. ტემპერატურის მატება იწვევს ნახშირბად-ნახშირბადის ბმის ჰომლიზურ რღვევას და თავისუფალი რადიკალების წარმოქმნას.
ეს რადიკალები ურთიერთქმედებენ ერთმანეთთან, წყალბადის ატომის გაცვლასთან ერთად მოლეკულის წარმოქმნით. ალკანის და ალკენის მოლეკულები:
თერმული დაშლის რეაქციები სამრეწველო პროცესის გულშია - ნახშირწყალბადის კრეკინგი. ეს პროცესი ნავთობის გადამუშავების ყველაზე მნიშვნელოვანი ეტაპია.
3. პიროლიზი. როდესაც მეთანი თბება 1000 °C ტემპერატურამდე, მეთანის პიროლიზი- დაშლა მარტივ ნივთიერებებად:
როდესაც თბება 1500 ° C ტემპერატურაზე, წარმოიქმნება აცეტილენი:
4. იზომერიზაცია. როდესაც ხაზოვანი ნახშირწყალბადები თბება იზომერიზაციის კატალიზატორით (ალუმინის ქლორიდი), წარმოიქმნება ნივთიერებები განშტოებული ნახშირბადის ჩონჩხი:

5. არომატიზაცია. ალკანები ექვსი ან მეტი ნახშირბადის ატომით ჯაჭვში კატალიზატორის თანდასწრებით ციკლირდება ბენზოლისა და მისი წარმოებულების წარმოქმნით:

ალკანები შედიან რეაქციებში, რომლებიც მიმდინარეობს თავისუფალი რადიკალების მექანიზმის მიხედვით, რადგან ალკანის მოლეკულებში ნახშირბადის ყველა ატომი sp 3 ჰიბრიდიზაციის მდგომარეობაშია. ამ ნივთიერებების მოლეკულები აგებულია კოვალენტური არაპოლარული C-C (ნახშირბადი - ნახშირბადი) ბმებისა და სუსტად პოლარული C-H (ნახშირბადი - წყალბადი) ბმების გამოყენებით. მათ არ აქვთ ელექტრონის მაღალი და დაბალი სიმკვრივის მქონე უბნები, ადვილად პოლარიზებადი ბმები, ანუ ისეთი ბმები, რომლებშიც ელექტრონის სიმკვრივე შეიძლება გადაინაცვლოს გარე ფაქტორების გავლენით (იონების ელექტროსტატიკური ველები). შესაბამისად, ალკანები არ რეაგირებენ დამუხტულ ნაწილაკებთან, ვინაიდან ალკანის მოლეკულებში ბმები ჰეტეროლიზური მექანიზმით არ იშლება.
ნახშირწყალბადები, რომელთა მოლეკულებში ატომები დაკავშირებულია ცალკეული ბმებით და რომლებიც შეესაბამება ზოგად ფორმულას C n H 2 n +2.
ალკანის მოლეკულებში ნახშირბადის ყველა ატომი sp 3 ჰიბრიდიზაციის მდგომარეობაშია. ეს ნიშნავს, რომ ნახშირბადის ატომის ოთხივე ჰიბრიდული ორბიტალი იდენტურია ფორმით, ენერგიით და მიმართულია ტოლგვერდა სამკუთხა პირამიდის - ტეტრაედრის კუთხეებისკენ. ორბიტალებს შორის კუთხეებია 109° 28'.
თითქმის თავისუფალი ბრუნვა შესაძლებელია ერთი ნახშირბად-ნახშირბადის ბმის ირგვლივ და ალკანის მოლეკულებს შეუძლიათ მიიღონ მრავალფეროვანი ფორმები ნახშირბადის ატომების კუთხით ოთხკუთხედთან ახლოს (109 ° 28 ′), მაგალითად, მოლეკულაში. ნ- პენტანი.

განსაკუთრებით ღირს ალკანების მოლეკულებში არსებული ბმების გახსენება. გაჯერებული ნახშირწყალბადების მოლეკულებში ყველა ბმა ერთია. გადახურვა ხდება ღერძის გასწვრივ,
ატომების ბირთვების დამაკავშირებელი, ანუ, ეს არის σ-ბმები. ნახშირბად-ნახშირბადის ბმები არაპოლარული და ცუდად პოლარიზებადია. C-C ბმის სიგრძე ალკანებში არის 0,154 ნმ (1,54 10 - 10 მ). C-H ობლიგაციები გარკვეულწილად მოკლეა. ელექტრონის სიმკვრივე ოდნავ გადადის უფრო ელექტროუარყოფითი ნახშირბადის ატომისკენ, ანუ C-H ბმა სუსტად პოლარულია.
გაჯერებული ნახშირწყალბადების მოლეკულებში პოლარული ბმების არარსებობა იწვევს იმ ფაქტს, რომ ისინი ცუდად იხსნება წყალში და არ ურთიერთქმედებენ დამუხტულ ნაწილაკებთან (იონებთან). ალკანებისთვის ყველაზე დამახასიათებელია რეაქციები, რომლებიც მოიცავს თავისუფალ რადიკალებს.
მეთანის ჰომოლოგიური სერია
ჰომოლოგები- სტრუქტურით და თვისებებით მსგავსი ნივთიერებები და განსხვავდებიან ერთი ან მეტი CH 2 ჯგუფით.

იზომერიზმი და ნომენკლატურა
ალკანებს ახასიათებს სტრუქტურული იზომერიზმი ე.წ. სტრუქტურული იზომერები ერთმანეთისგან განსხვავდებიან ნახშირბადის ჩონჩხის აგებულებით. უმარტივესი ალკანი, რომელიც ხასიათდება სტრუქტურული იზომერებით, არის ბუტანი. 
ნომენკლატურის საფუძვლები
1. მთავარი წრედის შერჩევა.ნახშირწყალბადის სახელის ფორმირება იწყება მთავარი ჯაჭვის განსაზღვრით - ნახშირბადის ატომების ყველაზე გრძელი ჯაჭვი მოლეკულაში, რაც, როგორც იქნა, მისი საფუძველია.
2. ძირითადი ჯაჭვის ატომების ნუმერაცია.მთავარი ჯაჭვის ატომებს ენიჭებათ რიცხვები. ძირითადი ჯაჭვის ატომების ნუმერაცია იწყება შემცვლელთან ყველაზე ახლოს ბოლოდან (სტრუქტურები A, B). თუ შემცვლელები ჯაჭვის ბოლოდან თანაბარ მანძილზე არიან, მაშინ ნუმერაცია იწყება ბოლოდან, სადაც მეტია (სტრუქტურა B). თუ სხვადასხვა შემცვლელი ჯაჭვის ბოლოებიდან თანაბარ მანძილზეა, მაშინ ნუმერაცია იწყება იმ ბოლოდან, რომელთანაც უფრო ძველია (სტრუქტურა G). ნახშირწყალბადების შემცვლელების ასაკი განისაზღვრება თანმიმდევრობით, რომლითაც იწყება მათი სახელი ანბანში: მეთილი (-CH 3), შემდეგ ეთილის (-CH 2 -CH 3), პროპილი (-CH 2 -CH 2 -CH 3) და ა.შ.
გაითვალისწინეთ, რომ შემცვლელის სახელი წარმოიქმნება სუფიქსის -an სუფიქსით - ჩანაცვლებით. სილაშესაბამისი ალკანის სახელით.
3. სახელის ფორმირება. სახელის დასაწყისში მითითებულია რიცხვები - ნახშირბადის ატომების რიცხვები, რომლებზეც განლაგებულია შემცვლელები. თუ მოცემულ ატომზე არის რამდენიმე შემცვლელი, მაშინ სახელში შესაბამისი რიცხვი მეორდება ორჯერ მძიმით გამოყოფილი (2,2-). ნომრის შემდეგ დეფისი მიუთითებს შემცვლელთა რაოდენობაზე ( დი- ორი, სამი- სამი, ტეტრა- ოთხი, პენტა- ხუთი) და შემცვლელის სახელწოდება (მეთილი, ეთილი, პროპილი). შემდეგ სივრცეებისა და დეფისების გარეშე - მთავარი ჯაჭვის სახელი. მთავარ ჯაჭვს მოიხსენიებენ, როგორც ნახშირწყალბადს - მეთანის ჰომოლოგიური სერიის წევრი ( მეთანი CH 4, ეთანი C 2 H 6, პროპანი C 3 H 8, C 4 H 10, პენტანი C 5 H 12, ჰექსანი C 6 H 14, ჰეპტანი C 7 H 16, ოქტანი C 8 H 18, ნონანი C 9 H 20, დეკანი C 10 H 22).

ალკანების ფიზიკური თვისებები
მეთანის ჰომოლოგიური სერიის პირველი ოთხი წარმომადგენელი არის აირები. მათგან უმარტივესი არის მეთანი - უფერო, უგემოვნო და უსუნო გაზი („გაზის“ სუნი, რომელსაც იგრძნობთ, რომელიც უნდა დარეკოთ 04-ზე, განისაზღვრება მერკაპტანების სუნით - გოგირდის შემცველი ნაერთები, რომლებიც სპეციალურად ემატება მეთანს, რომელიც გამოიყენება მეთანში. საყოფაცხოვრებო და სამრეწველო გაზის მოწყობილობები, რათა მათ ახლოს მყოფ ადამიანებს შეეძლოთ გაჟონვის სუნი).
ნახშირწყალბადები შემადგენლობის C 4 H 12-დან C 15 H 32-მდე - სითხეები; მძიმე ნახშირწყალბადები არის მყარი. ალკანების დუღილის და დნობის წერტილები თანდათან იზრდება ნახშირბადის ჯაჭვის სიგრძის მატებასთან ერთად. ყველა ნახშირწყალბადები ცუდად ხსნადია წყალში; თხევადი ნახშირწყალბადები ჩვეულებრივი ორგანული გამხსნელებია.
ალკანების ქიმიური თვისებები
ჩანაცვლების რეაქციები.
ალკანებისთვის ყველაზე დამახასიათებელია თავისუფალი რადიკალების შემცვლელი რეაქციები, რომლის დროსაც წყალბადის ატომი იცვლება ჰალოგენის ატომით ან რომელიმე ჯგუფით. წარმოვადგინოთ დამახასიათებელი რეაქციების განტოლებები ჰალოგენაცია: 
ჰალოგენის სიჭარბის შემთხვევაში, ქლორირება შეიძლება უფრო შორს წავიდეს, წყალბადის ყველა ატომის ქლორით ჩანაცვლებამდე: 
მიღებული ნივთიერებები ფართოდ გამოიყენება როგორც გამხსნელები და საწყისი მასალები ორგანულ სინთეზში.
დეჰიდროგენაციის რეაქცია(წყალბადის გაყოფა).
ალკანების კატალიზატორზე (Pt, Ni, Al 2 0 3, Cr 2 0 3) გავლის დროს მაღალ ტემპერატურაზე (400-600 ° C), წყალბადის მოლეკულა იყოფა და წარმოიქმნება ალკენი:
რეაქციები, რომელსაც თან ახლავს ნახშირბადის ჯაჭვის განადგურება.
ყველა გაჯერებული ნახშირწყალბადი იწვის ნახშირორჟანგის და წყლის წარმოქმნით. აირისებრი ნახშირწყალბადები, რომლებიც შერეულია ჰაერთან გარკვეული პროპორციებით, შეიძლება აფეთქდეს.
1. გაჯერებული ნახშირწყალბადების წვაარის თავისუფალი რადიკალების ეგზოთერმული რეაქცია, რომელიც ძალიან მნიშვნელოვანია ალკანების საწვავად გამოყენებისას:
ზოგადად, ალკანების წვის რეაქცია შეიძლება დაიწეროს შემდეგნაირად:
2. ნახშირწყალბადების თერმული გაყოფა.
პროცესი მიმდინარეობს თავისუფალი რადიკალების მექანიზმის მიხედვით. ტემპერატურის მატება იწვევს ნახშირბად-ნახშირბადის ბმის ჰომლიზურ რღვევას და თავისუფალი რადიკალების წარმოქმნას.
ეს რადიკალები ურთიერთქმედებენ ერთმანეთთან, წყალბადის ატომის გაცვლით, ალკანის მოლეკულის და ალკენის მოლეკულის წარმოქმნით:
თერმული გაყოფის რეაქციები საფუძვლად უდევს სამრეწველო პროცესს - ნახშირწყალბადების კრეკინგი. ეს პროცესი ნავთობის გადამუშავების ყველაზე მნიშვნელოვანი ეტაპია.
3. პიროლიზი. როდესაც მეთანი თბება 1000 ° C ტემპერატურამდე, იწყება მეთანის პიროლიზი - დაშლა მარტივ ნივთიერებებად: ![]()
1500 ° C ტემპერატურამდე გაცხელებისას შესაძლებელია აცეტილენის წარმოქმნა:
4. იზომერიზაცია. როდესაც ხაზოვანი ნახშირწყალბადები თბება იზომერიზაციის კატალიზატორით (ალუმინის ქლორიდი), წარმოიქმნება ნივთიერებები განშტოებული ნახშირბადის ჩონჩხით: 
5. არომატიზაცია. ალკანები ექვსი ან მეტი ნახშირბადის ატომით ჯაჭვში კატალიზატორის თანდასწრებით ციკლირდება ბენზოლისა და მისი წარმოებულების წარმოქმნით: 
ალკანები შედიან რეაქციებში, რომლებიც მიმდინარეობს თავისუფალი რადიკალების მექანიზმის მიხედვით, რადგან ალკანის მოლეკულებში ნახშირბადის ყველა ატომი sp 3 ჰიბრიდიზაციის მდგომარეობაშია. ამ ნივთიერებების მოლეკულები აგებულია კოვალენტური არაპოლარული C-C (ნახშირბადი - ნახშირბადი) ბმებისა და სუსტად პოლარული C-H (ნახშირბადი - წყალბადი) ბმების გამოყენებით. მათ არ აქვთ ელექტრონის მაღალი და დაბალი სიმკვრივის მქონე უბნები, ადვილად პოლარიზებადი ბმები, ანუ ისეთი ბმები, რომლებშიც ელექტრონის სიმკვრივე შეიძლება გადაინაცვლოს გარე ფაქტორების გავლენით (იონების ელექტროსტატიკური ველები). შესაბამისად, ალკანები არ რეაგირებენ დამუხტულ ნაწილაკებთან, ვინაიდან ალკანის მოლეკულებში ბმები ჰეტეროლიზური მექანიზმით არ იშლება. 
გაკვეთილი ნომერი 7.
გაკვეთილის თემა: „ბუნებრივი აირი.ალკანები».
გაკვეთილის მიზნები:1) საგანმანათლებლო: სტუდენტები უნდა ისწავლოს:გაჯერებული ნახშირწყალბადების კონცეფცია, მათი ქიმიური, სივრცითი და ელექტრონული აგებულება; მეთანისა და მისი ჰომოლოგების განხილვის მაგალითზე - ქიმიური ბმების ელექტრონული ბუნება და ნახშირწყალბადების მოლეკულების სივრცითი სტრუქტურა; ალკანების ლაბორატორიული და სამრეწველო წარმოების ძირითადი მეთოდები; გაჯერებული ნახშირწყალბადების ფიზიკური თვისებები.
2) განვითარება: სტუდენტები უნდა ისწავლოს:ახსნას მეთანის მოლეკულის ტეტრაედრული სტრუქტურა, გაჯერებული ნახშირწყალბადების ზიგზაგის ჯაჭვის სტრუქტურა; ჩამოწერეთ გაჯერებული ნახშირწყალბადების მოლეკულური, სტრუქტურული და ელექტრონული ფორმულები, დაასახელეთ სისტემატური ნომენკლატურის მიხედვით და შეადგინეთ ფორმულები სახელწოდებით;
3) საგანმანათლებლო: სტუდენტები უნდა დავრწმუნდეთ:მსოფლმხედველობის კონცეფციებში ბუნების შემეცნების შესახებ, მიზეზ-შედეგობრივი კავშირი გაჯერებული ნახშირწყალბადების შემადგენლობას, სტრუქტურას, თვისებებსა და გამოყენებას შორის და ა.შ. რომ ბუნება ქიმიური ბმაიგივეა როგორც არაორგანული, ისე ორგანული ნივთიერებებისთვის, რაც ამ ნივთიერებების ერთიანობის ერთ-ერთი დასტურია; „საყოფაცხოვრებო“ გაზის გამოყენების წესების დაცვის აუცილებლობაში მისი ფეთქებადობის გამო.
გაკვეთილზე შესწავლილი ძირითადი ცნებები:გაჯერებული ნახშირწყალბადები, ჰომოლოგები, ჰომოლოგიური სერიები, ჰომოლოგიური განსხვავება, ზოგადი ფორმულა, ელექტრონული ფორმულა, ნივთიერების მოლეკულების სივრცითი სტრუქტურა, მეთანის მოლეკულების ტეტრაედრული სტრუქტურა.
დაგეგმილი სწავლის შედეგები:შეძლოს მეთანის სერიის ნახშირწყალბადების მაგალითის გამოყენებით დაადგინოს, თუ როგორ განსხვავდება ყოველი მომდევნო ნახშირწყალბადები წინაგან მოლეკულების შემადგენლობით; შეადგინეთ ამ სერიის პირველი 4-5 ნახშირწყალბადის სტრუქტურული ფორმულები, მოიყვანეთ ამ ნივთიერებების იზომერების მაგალითები; განსაზღვრეთ გაჯერებული ნახშირწყალბადების მოლური მასა მათი ფორმულების მიხედვით, მიეცით ისტორიული სახელები; კონკრეტული მაგალითების გამოყენებით გაჯერებული ნახშირწყალბადების მოლეკულების და მათი ზოგიერთი იზომერის ელექტრონული და სივრცითი სტრუქტურის ასახსნელად; ნახშირწყალბადების სტრუქტურული და ელექტრონული ფორმულების შედგენა მოლეკულაში ნახშირბადის ატომების რაოდენობისა და მათი მოდელების მიხედვით.
მეთოდი:პრობლემური საუბარი ჰიპოთეზებთან; პრობლემური სიტუაციის სიმულაცია, რათა შემდეგ გაირკვეს ნახშირწყალბადების შემადგენლობის რეგულარული ცვლილების მიზეზი CH 2 ჯგუფში, ნახშირბადის ვალენტობის აშკარა დარღვევა, ორგანული ნაერთების მრავალფეროვნება; გაკვეთილზე მასალის ახსნისას პროგრამით მოთხოვნილი ლაბორატორიული ექსპერიმენტების დემონსტრირება.
აღჭურვილობა და რეაგენტები:სადემონსტრაციო მაგიდაზე ნახშირწყალბადების ნაკრები: ზეთი, ბენზინი (ნავთი), პროპან-ბუტანის ნარევი (თხევადი გაზი ქილაში), ძრავის ზეთი, ვაზელინი, პარაფინი (სანთელი), პოლიეთილენის პროდუქტები; კოვალენტური და იონური ბმების წარმოქმნის საჩვენებელი სქემები, მოხსნადი ტეტრაედრული მოდელი, მეთანისა და სხვა ნახშირწყალბადის მოლეკულების მასშტაბური და ბურთულა-ჯოხის მოდელები; გაზის სანთებელა გამჭვირვალე ავზით; კრისტალური CH 3 COONa, NaOH, KMnO 4, აირების მოსაპოვებელი მოწყობილობა, საცდელი მილები; ცხრილი: მეთანის სერიის ნახშირწყალბადები; მოსწავლეთა მაგიდებზე: ნაკრები მოლეკულების მოდელირებისთვის; სტიუარტ-ბრიგლების მოლეკულების მოდელები.
გაკვეთილების დროს.
1. საორგანიზაციო მომენტი.
2. ახალი მასალის შესწავლა.
მე. ნახშირწყალბადების კონცეფცია.
მასწავლებელი იწვევს ბავშვებს „გაშიფრონ“ ტერმინი ნახშირწყალბადი. ეს არ არის რთული: ნახშირწყალბადებს უწოდებენ ორგანულ ნაერთებს, რომლებიც შედგება ორი ელემენტის - ნახშირბადისა და წყალბადის ატომებისგან. ეს არის უმარტივესი ორგანული ნივთიერებები, რაც მათ მნიშვნელობას არ აკლებს. პირიქით, გერმანელი ქიმიკოსის კარლ შორლემერის განმარტებით, „ორგანული ქიმია არის ნახშირწყალბადების და მათი წარმოებულების ქიმია“.
ნახშირწყალბადების ზოგადი ფორმულა შეიძლება წარმოდგენილი იყოს როგორც C xჰ წ, სადაც Xდა ზეურთიერთდაკავშირებულია გარკვეული თანაფარდობით, რომელიც განსაზღვრავს ნახშირწყალბადების კლასს. ერთადერთ ნახშირწყალბადს - მეთანს - აქვს ერთი ნახშირბადის ატომი თავის შემადგენლობაში; სხვა ნახშირწყალბადებში, რიცხვი Xმერყეობს ორიდან რამდენიმე ათასამდე.
ორგანული ნივთიერებების ზოგადი კლასიფიკაცია, რომელიც განხილულია სახელმძღვანელოს § 5-ში (იხ. წინამდებარე სახელმძღვანელოს ნახ. 1), შეიძლება გავრცელდეს ნახშირწყალბადებზე. მასწავლებელი ყურადღებას ამახვილებს იმაზე, რომ ნახშირწყალბადების შესწავლა იწყება უმარტივესი კლასით - აციკლური გაჯერებული ნაერთებით, რომელსაც ალკანები ეწოდება.
II. მეთანის მოლეკულის ელექტრონული და სივრცითი სტრუქტურა.
უმარტივესი ნახშირწყალბადი - მეთანი - ხალხისთვის ცნობილია ძალიან დიდი ხნის განმავლობაში. ჭაობი ან მაღაროს გაზი ერქვა.
მეთანში ნახშირბადის ატომი sp 3 ჰიბრიდიზაციის მდგომარეობაშია. მოსწავლეებს ახსოვთ, რომ ნახშირბადს ამ შემთხვევაში აქვს ოთხი ეკვივალენტური ჰიბრიდული ორბიტალი, რომელთა ღერძები მიმართულია რეგულარული ტეტრაედრის წვეროებზე. ამ ორბიტალების ღერძებს შორის კუთხე არის 109°28". მასწავლებელი დაფაზე ასახავს ნახშირბადის ატომის სტრუქტურას sp 3 ჰიბრიდულ მდგომარეობაში.
მნიშვნელოვანია ხაზგასმით აღვნიშნოთ, რომ ნახშირბადის ატომის ელექტრონული სტრუქტურა განსაზღვრავს ატომების სივრცით განლაგებას მეთანის მოლეკულაში. ოთხივე კოვალენტური S-N კავშირებიწარმოიქმნება ნახშირბადის ატომის sp 3 -ორბიტალებისა და წყალბადის s-ორბიტალების გადაფარვით. მეთანის მოლეკულაში ყველა ბმა არის σ ტიპის. წყალბადის ატომების ბირთვების ცენტრები დევს რეგულარული ტეტრაედრის, ვალენტობის წვეროებზე. კუთხე H-S-Hარის 109°28.

მეთანის სივრცითი სტრუქტურის უფრო სპეციფიკური აღქმისთვის მასწავლებელი აჩვენებს მოლეკულის სამგანზომილებიან მოდელს (ბურთი და ჯოხი ან სტიუარტ-ბრიგლები), აძლევს ბავშვებს საშინაო დავალებას ასანთიდან და პლასტილინის ბურთებიდან მსგავსი მოდელის შეკრება.
III. გაჯერებული ნახშირწყალბადების ჰომოლოგიური სერია.
მასწავლებელი გაკვეთილის ამ ნაწილს იწყებს ხსენებით უნიკალური ქონებანახშირბადის ატომები ქმნიან გრძელ ჯაჭვებს ერთმანეთთან შეერთებით. თუ ნახშირბადის ყველა დარჩენილი ვალენტობა დაკავებულია წყალბადის ატომებით, ეს იქნება ნახშირწყალბადები, რომლებსაც ჩვეულებრივ უწოდებენ გაჯერებულს, პარაფინურს, გაჯერებულს ან ალკანებს. მასწავლებელი აძლევს ალკანების განმარტებას და შიფრავს ყველა სინონიმის მნიშვნელობას.
სიტყვა "ლიმიტი" ნიშნავს, რომ ნახშირბადის ატომები დაკავშირებულია წყალბადის ატომების მაქსიმალურ (ზღვრულ) რაოდენობასთან. გაჯერებული ნახშირწყალბადი არ შეიცავს ორმაგ ან სამმაგ ნახშირბად-ნახშირბადოვან კავშირებს. ტერმინი "პარაფინი" მომდინარეობს ლათინური ფრაზიდან პარუმი აფინისი, რაც ნიშნავს რომელსაც არ აქვს ნათესაობა.
ამრიგად, გაჯერებული ნახშირწყალბადები ქმნიან სპეციალურ ჯგუფს, ორგანული ნაერთების კლასს. ჰომოლოგიური სერიის ცნების გამეორებაზე გადასვლისას მასწავლებელი აკეთებს შემდეგ ანალოგიას. ცოდნის ნებისმიერ დარგს აქვს განყოფილება ე.წ ტაქსონომია(სიტყვასიტყვით: მოწესრიგება, კანონის მიხედვით). ის დაკავებულია იმ ობიექტების კლასიფიკაციით, რომლებსაც ეს მეცნიერება სწავლობს. ბიოლოგიაში, მაგალითად, ცხოველების ტიპები იყოფა კლასებად, კლასებად - რიგებად, ისინი - ოჯახებად, რომლებიც იყოფა გვარებად, გვარი იყოფა სახეობებად. არაორგანულ ქიმიაში არის ნივთიერებების დაყოფა კლასებად. რომელი? მოსწავლეები ასახელებენ ოქსიდებს, ფუძეებს, მჟავებს, მარილებს. ამ კლასებში არის გრადაცია. ორგანულ ქიმიაში მოცემული კლასის ყველა ნივთიერება შეიძლება განლაგდეს რიგად, რომელსაც ეწოდება ჰომოლოგიური. მოდით, ნახშირბადის ორმა ატომმა შექმნას კოვალენტური არაპოლარული ბმა ერთმანეთთან. თითოეულს აქვს სამი თავისუფალი ვალენტობა, დაუწყვილებელი ელექტრონები. თუ ყველა ეს ვალენტური შესაძლებლობა წყალბადის ატომებით არის გაჯერებული, მივიღებთ ნახშირწყალბადს ეთანი.ანალოგიურად, მასწავლებელი აშენებს მოლეკულას პროპანი:
| | | | | | | | | |
– C – C – → H – C – C – H – C – C – C – → H – C – C – C – H
| | | | | | | | | |
ვინაიდან მოლეკულების სტრუქტურა მსგავსია, მათი ქიმიური თვისებებიც მსგავსია. რა განსხვავებაა ამ ნივთიერებების შემადგენლობაში? სტრუქტურული ფორმულებიდან აშკარად ჩანს, რომ ისინი განსხვავდებიან ჯგუფით - CH 2 - ერთი ან მეტი.
ჰომოლოგიური სერიაეწოდება ორგანული ნაერთების ერთობლიობას, რომლებსაც აქვთ მსგავსი აგებულება და თვისებები და შემადგენლობით განსხვავდებიან ერთი ან მეტი ჯგუფით - CH 2 - (ჰომოლოგიური განსხვავება). იგივე ჰომოლოგიური სერიის წევრებს ეძახიან ჰომოლოგები.
მასწავლებლის მცირე დახმარებით, რომელმაც პროპანის მოლეკულა ფრაგმენტებად „დაყო ხვეული ბრეკეტებით“, ბიჭები ასკვნიან. ზოგადი ფორმულაალკანები: C n H 2 n +2.
H-C-C-C-H
H + C n H 2n + H
ზემოთ მოცემული ეთანისა და პროპანის ფორმულები ე.წ სრული სტრუქტურული ფორმულები. ყველაზე ხშირად, არ არის საჭირო მატერიის სტრუქტურის ასე დეტალურად გამოსახვა. საკმაოდ ინფორმაციული შემოკლებულიარ არის ნაჩვენები სტრუქტურული ფორმულები, რომლებშიც C-H ბმები "დაკეცილია". აღნიშნული ეთანისა და პროპანისთვის ისინი ნაცნობია: CH 3 - CH 3 და CH 3 - CH 2 - CH 3 ან თუნდაც CH 3 CH 3 და CH 3 CH 2 CH 3. მნიშვნელოვანია აღინიშნოს, რომ ორივე ვარიანტი ექვივალენტურია. მართლაც, როგორც წესი, მასწავლებელი დიდ მნიშვნელობას არ ანიჭებს შემოკლებული სტრუქტურული ფორმულის დაწერის ამა თუ იმ ხერხს და ბიჭები ცდილობენ გაიხსენონ, საჭიროა თუ არა ფორმულაში „ინსულტი“.
ორგანული ნივთიერებების მიმართვის კიდევ ერთი გზაა მოლეკულური ფორმულები. ისინი მხოლოდ აჩვენებენ ნაერთიმოლეკულები, მაგრამ არ აირეკლება ლინკის შეკვეთაატომები. ეთანს აქვს მოლეკულური ფორმულა C 2 H 6 , პროპანი C 3 H 8 . მასწავლებელი ამოწმებს, თუ როგორ შეასრულეს ბავშვებმა დავალება, გააკეთონ ბარათები ალკანების ჰომოლოგიური სერიის პირველი 10 წევრის სახელებითა და ფორმულებით, სთხოვს მათ, რომ ეს ბარათები მოიყვანონ მომდევნო გაკვეთილებზე.
IV. ალკანების იზომერიზმი და ნომენკლატურა.
ამ გაკვეთილის ძალიან მნიშვნელოვანი ამოცანაა ბავშვებს ასწავლონ ჰომოლოგებისა და იზომერების სტრუქტურული ფორმულების შედგენა. შეიძლება ამ გზით მიახლოება. მასწავლებელი, მოლეკულების მასშტაბური მოდელების გამოყენებით, გვთავაზობს დაბრუნებას ალკანების ჰომოლოგიური სერიის წინაპართან - მეთანთან. ყველა CH ბმა მოლეკულაში ექვივალენტურია. თუ ამ ბმებიდან ერთ-ერთი დაირღვა ისე, რომ თითოეულმა ატომმა დაიბრუნოს თავისი ადრე გაზიარებული ელექტრონი, წარმოიქმნება ორი ნაწილაკი: წყალბადის ატომი და მეთილის რადიკალი. რა ჰქვია ამ ბმის რღვევას ორგანულ ქიმიაში? ეს არის ჰემოლიზური რღვევა. ახლა მოდით გავაერთიანოთ ორი ლითონის რადიკალი. ვიღებთ მეთანის ჰომოლოგს - ეთანს. ამ ნახშირწყალბადში, ისევე როგორც მეთანში, წყალბადის ყველა ატომი ექვივალენტურია. რომელიმე მათგანის მეთილის რადიკალით ჩანაცვლებით, ვიღებთ კომპოზიციის ერთადერთ მესამე ჰომოლოგს C 3 H 8 - პროპანს. წყალბადის ატომები ამ ალკანში აღარ არის იგივე: ექვსი მათგანი განლაგებულია ნახშირბადის უკიდურეს ატომებზე, ხოლო ორი მდებარეობს შუაში. თუ ჩვენ ოფიციალურად შევცვლით H ექვსი „ექსტრემალური“ ატომიდან რომელიმეს რადიკალით CH 3 -, მივიღებთ ნორმალური სტრუქტურის ბუტანს - ნ-ბუტანი. თუ წყალბადის ორი „ცენტრალური“ ატომიდან ერთს ექვემდებარება ასეთი ჩანაცვლება, ეს უკვე განსხვავებული მოლეკულაა, იგივე შემადგენლობის სხვა ნივთიერება C 4 H 10 არის იზობუტანი. H H H H
H-C-C-C-C-H
H H H H H H | | | |
| | | | | | a H H H H
H – C–– H → H – C – C ––H → H – C – C – C–– H ა
| | | | | ბ | H H H
H H H H H H | | |
H-C-C-C-H
მასწავლებელი ეკითხება, რა ჰქვია ნივთიერებებს, რომლებსაც აქვთ იგივე შემადგენლობა, მაგრამ განსხვავებული ქიმიური სტრუქტურა? რა თქმა უნდა, ეს არის იზომერები. და აქ კიდევ ერთხელ ფიქსირდება სტრუქტურული იზომერიზმის ცნებები.
ბუტანის იზომერებს აქვთ ატომების სხვადასხვა შემაკავშირებელი რიგი მოლეკულაში. ის სტრუქტურული იზომერიზმი.
ამ სახის სტრუქტურული იზომერიზმი, რომელშიც ერთი და იგივე ჰომოლოგიური სერიის წარმომადგენლები განსხვავდებიან მოლეკულაში ნახშირბადის ატომების შეერთების თანმიმდევრობით, ე.წ. ნახშირბადის ჩონჩხის იზომერიზმი.
n-ბუტანისა და იზობუტანისგან ანალოგიურად აგებული პენტანის იზომერების მაგალითის გამოყენებით მასწავლებელი აძლიერებს განსხვავებას „იზომერის“ და „ჰომოლოგის“ ცნებებში. ნებისმიერი ორი ბუტანიდან რომელიმე პენტანთან მიმართებაში არის ჰომოლოგიური, მაგრამ არა იზომერი! პენტანები ერთმანეთში იზომერებით "მოაქვთ", მაგრამ არ არიან ჰომოლოგები.
პენტანის იზომერები ბუტანის იზომერები
H H H H H H H H H
| | | | | | | | | |
H – C – C – C – C – C – C – H H – C – C – C – C – H
| | | | | | | | | |
H H H H H H H H H
ჰომოლოგები
CH 3 - CH - CH 2 - CH 3 CH 3 - CH - CH 3
ჰომოლოგები
H-C-C-C-H
ამ ეტაპზე მიზანშეწონილია ცნებების გაცნობა პირველადი, მეორადი, მესამეული და მეოთხეულინახშირბადის ატომები დაფაზე გამოსახული სტრუქტურების მაგალითზე. ეს კლასიფიკაცია ეფუძნება მონაცემებთან დაკავშირებული მეზობელი ნახშირბადის ატომების რაოდენობას. ნორმალურ პენტანს აქვს ორი პირველადი და სამი მეორადი ნახშირბადის ატომები; იზოპენტანი - სამი პირველადი, ერთი მეორადი და ერთი მესამეული ატომი; ბოლო იზომერს აქვს ოთხი პირველადი და ერთი მეოთხეული ნახშირბადის ატომი.
იმისათვის, რომ სტუდენტებმა დაწერონ მითითებული კომპოზიციის ყველა შესაძლო იზომერის ფორმულები, რომ არ იყოს ასახული არასაჭირო სტრუქტურები, და ასევე თავიდან აიცილონ ზოგიერთი ჩვეულებრივი შეცდომა ალკანების ნომენკლატურაში, სასარგებლოა შემდეგი ახსნა მოლეკულის მოდელის გამოყენებით ( მაგალითად, იზოპენტანი). რეალური მოლეკულა იკავებს ნებისმიერ პოზიციას და ფორმას სივრცეში, რაც საშუალებას აძლევს მას თავისუფლად ბრუნოს C - C ბმებთან მიმართებაში. ჩვენ შეგვიძლია გამოვსახოთ მისი სტრუქტურული ფორმულა სიბრტყეზე (დაფაზე ან რვეულში) თვითნებურად, ჩვენთვის მოსახერხებელი გზით. . აქედან იზოპენტანი არ შეწყვეტს იზოპენტანობას, არ გადაიქცევა სხვა იზომერად.
ეს ყველაფერი პენტანებია!
CH 3 CH 3 CH 3 CH 3
CH 3 - CH - CH 2 - CH 3 CH 3 - CH CH - CH 2 CH 2 - CH - CH 3 CH - C 2 H 5
CH 2 CH 3 CH 3 CH 3 CH 3 CH 3
იმისათვის, რომ ცალსახა იყოს თითოეული ნივთიერების საკუთარი სახელის მინიჭება და სახელით შესაძლებელი იყო ნივთიერების ფორმულის რეპროდუცირება, შეახსენებს მასწავლებელს, ქიმიკოსები იყენებენ სახელების სპეციალურ სისტემას - ქიმიურ ნომენკლატურას და ხაზს უსვამენ, რომ სტუდენტები უკვე ვიცით, რომ ეს არის ყველაზე უნივერსალური და გასაგები ნებისმიერ ე.წ. საერთაშორისო ნომენკლატურაზე (IUPAC). მოსწავლეები ასახელებენ ნაჩვენები სტრუქტურებიდან პირველს და დარწმუნდებიან, რომ ყველა დანარჩენს ერთი და იგივე სახელი აქვს - 2-მეთილბუტანი. ეს იგივე ნივთია! პირიქითაც მართალია: თითოეული სახელი შეიძლება შეესაბამებოდეს ერთ სუბსტანციას.
მასწავლებელი ხაზს უსვამს, რომ ალკანების სახელების შედგენა და სტრუქტურული ფორმულების სახელებით გამოსახვა საინტერესო აქტივობაა. მით უმეტეს, თუ მოსწავლეები რაციონალურად მუშაობენ. ამისათვის თქვენ მკაცრად უნდა დაიცვან შემდეგი ალგორითმი.
1. აირჩიეთ ნახშირბადის ატომების ყველაზე გრძელი ჯაჭვი მოლეკულაში.
2. დანომრეთ ჯაჭვი მოლეკულის განშტოებამდე ყველაზე ახლოს ბოლოდან.
3. სახელის საფუძველია ნახშირწყალბადის სახელწოდება ნახშირბადის ატომების იგივე რაოდენობით, როგორც ყველაზე გრძელ ჯაჭვში (მინიშნებული ბარათი ეხმარება).
4. სახელწოდების ფუძის წინ ჩამოთვალეთ ძირითადი ჯაჭვის ყველა შემცვლელი ნახშირბადის ატომების რაოდენობის მითითებით, რომლებზეც ისინი დგანან. თუ არსებობს რამდენიმე იდენტური შემცვლელი, მათი სახელების წინ იდება პრეფიქსი di-, tri-, ტეტრა-და ა.შ.
5. ყველა რიცხვი ერთმანეთისგან გამოყოფილია მძიმეებით, ასოები რიცხვებიდან - დეფისით, სახელი იწერება ერთი სიტყვით (სივრცის გარეშე). თუ ნახშირბადის ერთ ატომს აქვს არა ერთი, არამედ ორი შემცვლელი, მისი რიცხვი ორჯერ მეორდება სახელში (მაგალითად, 2,2-დიმეთილბუტანი და არა 2-დიმეთილბუტანი).
ჩამოთვლილი წესები ილუსტრირებულია შემდეგი მაგალითებით:
CH 3 - CH 2 - CH 2 - CH 2 - CH 2 - CH 3 CH 3 - CH - CH 2 - CH 2 - CH 3
ნ-ჰექსანი |
2-მეთილპენტანი
CH 3 - C - CH 3 CH 3 - CH 2 - C - CH - CH 3
2,2-დიმეთილპროპანი 2,3,3-ტრიმეთილპენტანი
7 6 5 4 | 3 3 4 |
CH 3 - CH 2 - CH - CH - CH - CH 3 CH 3 - CH - CH - CH 3
C 2 H 5 CH 2 - CH 3 C 2 H 5
3,4-დიმეთილ-5-ეთილჰეპტანი 3, 4-დიეთილჰექსანი
ქიმიით განსაკუთრებით დაინტერესებულ მოსწავლეებს მასწავლებელი ახსენებს, რომ ხშირად ნახშირწყალბადების და რადიკალების დასახელებისას გამოიყენება სხვადასხვა ნომენკლატურის ზოგიერთი ტერმინი - რაციონალური.სასარგებლოა გვახსოვდეს, რომ თუ არსებობს CH 3 -CH (CH 3) ფრაგმენტი ალკანში ან ალკილის შემცვლელში, მის სახელს შეიძლება დაემატოს პრეფიქსი. იზო-, ფრაგმენტი CH 3 -C (CH 3) 2 - პრეფიქსი ნეო-:
CH 3 - CH - CH 3 CH 3 - C - CH 2 - CH 3
იზობუტანი ნეოჰექსანი
CH 3 - CH - CH 2 - CH 3 - CH -
იზობუტილის იზოპროპილი
მოსწავლეებს უნდა შეეძლოთ შემოთავაზებული შემადგენლობის ყველა იზომერული ნახშირწყალბადების სტრუქტურული ფორმულების შედგენა. ეს მოითხოვს გარკვეულ უნარს.
შესაძლო იზომერების ფორმულები უნდა იყოს გამოსახული, ნორმალური სტრუქტურის ერთი იზომერით დაწყებული. შემდეგ, ჯაჭვის თანმიმდევრულად შემცირება ერთი ნახშირბადის ატომით, გამოსახულია იზომერების ფორმულები განშტოებული ნახშირბადის ჩონჩხით. თუ პირველ წყვილში არის შეცდომები წყალბადის ატომების რაოდენობის დადგენაში, უმჯობესია ჯერ დახატოთ "შიშველი" ნახშირბადის ჩონჩხი (დაითვალოთ ნახშირბადის ატომები!), შემდეგ კი მასზე "დაკიდოთ" წყალბადის ატომები, იმის გათვალისწინებით. ნახშირბადის ატომის ოთხვალენტიანობა.
როგორ არ დავწეროთ "დამატებითი" იზომერული ფორმულები? აუცილებელია დაუყოვნებლივ დაასახელოთ გამოსახული ალკანი: არ უნდა იყოს ორი იდენტური სახელი.
სახელის მიხედვით სტრუქტურული ფორმულა კიდევ უფრო ადვილია გამოსახული. თქვენ უნდა დაიწყოთ სახელის საფუძვლით - "შიშველი" ნახშირბადის ატომების ჯაჭვი, რომელიც დანომრილია მარცხნიდან მარჯვნივ. შემდეგ თავსდება რადიკალები და ბოლოს წყალბადის ატომები ემატება ჯაჭვს ნახშირბადის ატომის ოთხვალენტურობის გათვალისწინებით.
ვ. ალკანების მიღების მეთოდები.
მასწავლებელი, ეყრდნობა არაორგანული ქიმიის კურსის მოსწავლეთა ცოდნას, იხსენებს, რომ ალკანების მიღების მეთოდები, ისევე როგორც სხვა პრაქტიკულად მნიშვნელოვანი ნივთიერებები, შეიძლება დაიყოს სამრეწველო და ლაბორატორიულებად (ნახ. 3).
ალკანების მიღების მეთოდები
სამრეწველო ლაბორატორია
იზოლაცია კრეკინგი იზომერიზმი-ჰიდრორეაქციის პიროლიზის ჰიდროლიზი
ბუნებიდან - ნავთობის წარმოების ვურცის კარბიდის მარილები
ალკანების წყაროები ალკენი ალკენები ალუმინი
მჟავების ნიკელი
ბუნებრივი ზეთი ასოცირებული
გაზის ნავთობის გაზები
ნახ.3. გაჯერებული ნახშირწყალბადების მიღების მეთოდები.
ინდუსტრიაში, ტექნოლოგიასა და ყოველდღიურ ცხოვრებაში ინდივიდუალური (ქიმიურად სუფთა) ნახშირწყალბადები იშვიათად გამოიყენება. საკმარისია მოლეკულური მასით ახლოს ალკანების ნარევი. მაგალითად, ბუნებრივი აირი ძირითადად შედგება მეთანისგან (88-95%), ეთანისგან (3-8%), პროპანისგან (0,7-2%) და ბუტანისგან (0,2-0,7%) არაორგანული აირების შერევით. ნავთობისგან პრაქტიკულად ღირებული ნივთიერებების მისაღებად მას ექვემდებარება გასწორება- წილადებად დაყოფა, რაც დეტალურად არის აღწერილი სახელმძღვანელოში. ფრაქცია არის ნივთიერებების ნარევი, რომელთა დუღილის წერტილები გარკვეულ წინასწარ განსაზღვრულ დიაპაზონშია.
ნავთობპროდუქტების სამრეწველო გადამუშავების პროცესების განხილვისას მასწავლებელი იწყებს გზავნილით, რომ ნავთობის პირდაპირი დისტილაციის ყველაზე ღირებული ფრაქცია არის ბენზინი. თუმცა ამ ფრაქციის გამოსავლიანობა ნედლი ნავთობის წონით 17-20%-ს არ აღემატება. ჩნდება პრობლემა: როგორ დავაკმაყოფილოთ საზოგადოების მზარდი მოთხოვნილებები საავტომობილო და საავიაციო საწვავზე? გამოსავალი მე-19 საუკუნის ბოლოს იქნა ნაპოვნი. რუსი ინჟინერი ვლადიმერ გრიგორიევიჩ შუხოვი. 1891 წელს მან პირველმა განახორციელა ნავთობის ნავთის ფრაქციის სამრეწველო კრეკინგი, რამაც შესაძლებელი გახადა ბენზინის მოსავლიანობის გაზრდა 65-70%-მდე (გათვლილი ნედლ ნავთობზე)! მხოლოდ ნავთობპროდუქტების თერმული კრეკინგის პროცესის განვითარებისთვის, მადლიერმა კაცობრიობამ ოქროს ასოებით ჩაიწერა ცივილიზაციის ისტორიაში ამ უნიკალური ადამიანის სახელი. თუმცა, ცოტამ თუ იცის, რომ შუხოვმა სარატოვში მდინარის ტანკერების ბარჟები შექმნა ნავთობის გადასატანად. პირველად მსოფლიოში ეს გემები აწყობილი იქნა ცალკეული განყოფილებებიდან, რამაც შესაძლებელი გახადა მათი მარაგებიდან გაშვება ძალიან მოკლე დროში. ბარჟის ჩასატვირთად და გადმოტვირთვისთვის, ვ. ბაქოს ნავთობის საბადოებში ვლადიმერ გრიგორიევიჩმა გამოიგონა პირველი მილსადენი ნავთობის სატუმბი გათბობით, რამაც შესაძლებელი გახადა მილის კედლებზე პარაფინის კრისტალიზაციის თავიდან აცილება და პარაფინის საცობების წარმოქმნა.
ნორმალური ალკანების იზომერიზაციის პროცესსაც უწოდებენ რეფორმირება.მას დიდი მნიშვნელობა აქვს ნედლი ნავთობის პირველადი დისტილაციის შემდეგ მიღებული ბენზინის ფრაქციის ხარისხის გასაუმჯობესებლად. კატალიზური იზომერიზაცია მიმდინარეობს იონური მექანიზმის მიხედვით.
მასწავლებელი ასრულებს პრობლემური სიტუაციის მქონე ალკანების მიღების სამრეწველო მეთოდების განხილვას. ნავთობის მოპოვება და მოხმარება დიდი ხანია წმინდა ეკონომიკური საკითხიდან სახელმწიფოთაშორისი პოლიტიკური ურთიერთობების განსაკუთრებულ ფორმად გადაიქცა. როგორც ჩანს, ნავთობის მწარმოებელი ქვეყნებისთვის ეკონომიკურად მომგებიანია ნავთობის მოპოვებისა და გაყიდვების გაზრდა. თუმცა ამ შემთხვევაში საქონელზე ფასები დაეცემა და მოგების ნაცვლად ზარალს მოიტანს. თითოეულ სახელმწიფოს აქვს გარკვეული კვოტა „შავი ოქროს“ გაყიდვების მოცულობისთვის, რაც სასტიკი ბრძოლის საგანია ნავთობის უმსხვილეს მონოპოლიებსა და წამყვან მრეწველებს შორის. განვითარებული ქვეყნები.
ამასთან, ნავთობის წარმოება და მოხმარება ყოველწლიურად იზრდება საშუალოდ 8%-ით. ექსპერტების აზრით, შესწავლილი რეზერვები მხოლოდ მომდევნო 50-70 წლის განმავლობაში გაგრძელდება. შესაძლებელია თუ არა თანამედროვე მცენარეული და ცხოველური ნაშთების გამოყენება, თუ არა ნავთობი, მაშინ მაინც გაზის (მას ე.წ ბიოგაზი)? გამოდის, რომ ეს სავსებით შესაძლებელია და უკვე დიდი მასშტაბით გამოიყენება ბევრ განვითარებად ქვეყანაში (ინდოეთი, ჩინეთი). ბიოგაზის ქარხნები იყენებენ ცხოველურ ნარჩენებს და მცენარეული წარმოშობა, რომლებიც გენერატორებში ანაერობული ბაქტერიების მოქმედებით ლპება (სურ. 4). ბუნებრივი აირის მსგავსად, ბიოგაზიც ძირითადად მეთანისგან შედგება. ის შეიძლება გამოყენებულ იქნას უშუალოდ სახლის გასათბობად, სამზარეულოსთვის ან ელექტროენერგიის გამომუშავებისთვის ელექტრო გენერატორის გამოყენებით. მცენარეული და ცხოველური ნარჩენების ნარჩენები ბიოგაზის წარმოების შემდეგ შეიძლება გამოყენებულ იქნას, როგორც ეკოლოგიურად ეფექტური სასუქები, რადგან ისინი შეიცავს მნიშვნელოვან რაოდენობას.
შეკრული აზოტი.
გენერატორი
ბოსტნეულის
ბიომასა
ან სასუქი
გენერატორი
სასუქები
ბრინჯი. 4. ბიოგაზის წარმოება და გამოყენება.
ალკანების მიღების ლაბორატორიული მეთოდებიდან ყველაზე გავრცელებულია სხვადასხვა ტიპის პრობლემებში ვურცის სინთეზიდა კარბოლის მჟავების მარილების პიროლიზიტუტეებით.
ფრანგმა ქიმიკოსმა, პარიზის მეცნიერებათა აკადემიის წევრმა ჩარლზ ადოლფ ვურცმა 1855 წელს შეიმუშავა უნივერსალური გზაგაჯერებული ნახშირწყალბადების სინთეზი ჰალოალკანების ლითონებით გახურებით (ნატრიუმი, თუთია მტვერი). სხვათა შორის, ზემოაღნიშნული რეაქციის გარდა, ს.ვურცმა დიდი წვლილი შეიტანა ორგანული ქიმიის განვითარებაში, მინერალი ვურციტი მის სახელს ატარებს.
სიცხადისთვის, Wurtz-ის რეაქციის განტოლებაში მასწავლებელი გვიჩვენებს, თუ როგორ წარმოიქმნება ლითონის მოქმედების შედეგად რადიკალები, რომლებიც ერთმანეთთან ერწყმის ახალი ალკანის მოლეკულას. ეს პროცესი ასევე შეიძლება მოხერხებულად იყოს გამოსახული მოლეკულური მოდელების დახმარებით.
CH 3 - CH 2 - Br Br - CH 2 - CH 3 CH 3 - CH 2 - CH 2 - CH 3 + 2NaBr
ძლიერი მოსწავლეები, ცხადია, შეძლებენ პრობლემური სიტუაციის გადაჭრას: „რა ნივთიერებები მიიღება, თუ ორი განსხვავებული ჰალოალკანი შევა ვურცის რეაქციაში? ცხადია, შესაძლებელია ორი ჰალოალკანის სამი განსხვავებული კომბინაცია, რამაც უნდა გამოიწვიოს სამი საბოლოო ნახშირწყალბადის სინთეზი:
CH 3 -Br Br - CH 3 CH 3 - CH 3
CH 3 - CH 2 - CH 3
CH 3 - CH 2 - Br Br - CH 2 - CH 3 CH 3 - CH 2 - CH 2 - CH 3
შებრუნებული პრობლემა უფრო რთულია სტუდენტებისთვის, მაგალითად: რომელი ჰალოალკანი უნდა იქნას მიღებული ვურცის რეაქციაში 2,3-დიმეთილბუტანის მისაღებად? გამოსავალი უკეთესია შესრულდეს საპირისპიროდან:
დახაზეთ სასურველი პროდუქტის ფორმულა
CH 3 - CH - CH - CH 3
გაყავით იგი ნახევრად (ორ რადიკალად)
CH 3 - CH - - CH - CH 3
დაამატეთ ჰალოგენის ატომი რადიკალებს
CH 3 - CH - Br CH 3 - CHBr - CH 3
ეს არის 2-ბრომოპროპანი:
2CH 3 - CHBr - CH 3 + 2Na CH 3 - CH - CH - CH 3 + 2NaBr
ვურცის რეაქციის თვალსაჩინო მახასიათებელია პროდუქტში ნახშირბადის ატომების რაოდენობის გაორმაგება საწყის მასალასთან შედარებით.
ალკანების მიღების სხვა ლაბორატორიული მეთოდის თავისებურებაა ნახშირბადის ატომების რაოდენობის შემცირება ერთით. ეს არის დაახლოებით პიროლიზი(ნივთიერების გათბობა, რაც იწვევს მის დაშლას) კარბოქსილის მჟავების მარილები ტუტეებით. მასწავლებელი აჩვენებს ამ რეაქციას ნატრიუმის აცეტატისა და ნატრიუმის ჰიდროქსიდის ნარევის გაცხელებით სინჯარაში გაზის მილით. სტუდენტები აცხადებენ, რომ მეთანი წყალში უხსნადია (ის შეიძლება შეგროვდეს სინჯარაში წყლის გადაადგილებით), არ აფერხებს კალიუმის პერმანგანატის ხსნარს და იწვის ღია ცისფერი ალით.
CH 3 - COONa + Na - O - H CH 4 + Na 2 CO 3
განტოლების მარცხენა ნახევრის დაფაზე დაწერის შემდეგ მასწავლებელი სთხოვს ბავშვებს დაადგინონ რომელი არაორგანული ნივთიერება (ყუთში შემოხაზული) გამოიყოფა ქვეპროდუქტის სახით (ნატრიუმის კარბონატი). შეიძლება გავიხსენოთ, რომ კარბოქსილის მჟავების ფუნქციურ ჯგუფს კარბოქსილი ეწოდება. ამ რეაქციაში კარბოქსილის მჟავას წარმოებული (მარილი) კარგავს კარბოქსილის ნაწილს, ამიტომ რეაქციას ეწოდება დეკარბოქსილაცია.
ალკანების წარმოების კონკრეტული მეთოდის მაგალითია ალუმინის კარბიდის ჰიდროლიზი. სიტყვა ჰიდროლიზის ეტიმოლოგია (ბერძნული სიტყვებიდან hydor - წყალი და lysis - დაშლა, დაშლა) საშუალებას გვაძლევს განვსაზღვროთ ისეთი რეაქციები, როგორიცაა რთული ნაერთის ორ ან მეტ ახალ ნივთიერებად დაშლის პროცესი წყლის გავლენის ქვეშ.
Al 4 C 3 + 12H 2 O → 4Al (OH) 3 + 3CH 4
VI. ალკანების ფიზიკური თვისებები.
მასწავლებელი ამახვილებს ბავშვების ყურადღებას იმ ფაქტზე, რომ ნებისმიერ ჰომოლოგიურ სერიაში ჯაჭვში ნახშირბადის ატომების რაოდენობის ზრდით (ანუ ფარდობითი მოლეკულური წონის მატებით), დნობის და დუღილის წერტილები და სიმკვრივე. ნივთიერებების გაზრდა. ეს არის ბუნების კანონის ერთ-ერთი დადასტურება რაოდენობის ხარისხში გადასვლის შესახებ. ამრიგად, ალკანები შეიძლება არსებობდეს აგრეგაციის სამ სხვადასხვა მდგომარეობაში. მოსწავლეებს ახსოვთ აგრეგატული მდგომარეობების ტიპები, მათ შორის განსხვავება მოლეკულათაშორისი ურთიერთქმედების და მოლეკულების მოწესრიგების ხარისხით. მასწავლებელი დაფაზე აჯამებს პასუხებს დიაგრამის ჩაწერით (სურ. 5).
მატერიის აგრეგატული მდგომარეობა
აირისებრი თხევადი მყარი
კრისტალური ამორფული
ბრინჯი. 5. მატერიის აგრეგატული მდგომარეობები.
მასწავლებელი აჩვენებს ალკანების ნიმუშებს. აირისებრი ნახშირწყალბადები არ არის ადვილი შესამჩნევი, მაგრამ პროპანი და ბუტანი უფერო სითხეებია წნევის ქვეშ მყოფი გაზის სანთებელში. როდესაც სარქველი დაჭერილია, უფერო აირისებრი ალკანები, თითქმის უსუნო, ოდნავ ჩურჩულით გამოდიან. თუ სანთებელას აანთებთ, მაშინ ალკანები იწვება ოდნავ შეღებილი ალით.
თხევად გაჯერებულ ნახშირწყალბადებს (ბენზინს) უკვე აქვთ სუნი. მასწავლებელი ასხამს რამდენიმე მილილიტრ ბენზინს სინჯარაში წყლით. ინტერფეისი ცუდად ჩანს, ორივე სითხე უფეროა. საცდელი მილის ენერგიული შერყევისას წარმოიქმნება მოღრუბლული ემულსია, რომელიც სწრაფად გამოყოფს: გაჯერებული ნახშირწყალბადები წყალში უხსნადია. თუ კალიუმის პერმანგანატის კრისტალს სინჯარაში ჩააგდებთ, წყლის ფენა შეღებილი გახდება. ფერი არ გაქრება, რადგან ალკანები არ რეაგირებენ KMnO 4-ის წყალხსნართან.
ვაზელინი არის თხევადი და მყარი გაჯერებული ნახშირწყალბადების ნარევი. ჩანს, რომ მაღალი მოლეკულური წონის ალკანები ცხიმიანია შეხებით. პარაფინი - მყარი ნახშირწყალბადების ნარევი, აქვს ამორფული მდგომარეობა. მასწავლებელი აჩვენებს, რომ პარაფინის ნაჭერი ცურავს წყლის ზედაპირზე (მისი სიმკვრივე ერთიანობაზე ნაკლებია) და ადვილად დნება (როდესაც საცდელ მილში წყალი გაცხელდება, პარაფინის ნაჭერი გადაიქცევა სითხეში). თუმცა, გაჯერებული ნახშირწყალბადები ადვილად იხსნება არაპოლარულ ორგანულ გამხსნელებში; თხევადი ალკანები შერეულია ერთმანეთთან.
ყველა აირისებრი და თხევადი ალკანი ქმნის ფეთქებად ნარევებს ჰაერთან, ამიტომ მათ ყოველდღიურ ცხოვრებაში ძალიან ფრთხილად უნდა მოექცეთ.
მასალის კონსოლიდაციისთვის რეკომენდებულია ალკანების მოპოვების მეთოდების შესახებ მრავალი პრობლემის გადაჭრა, აგრეთვე ელემენტების მასობრივი ფრაქციების საშუალებით ნივთიერების ფორმულის პოვნის ამოცანების გახსენება (გახსნის ალგორითმი მოცემულია მასწავლებლის წიგნში, კლასი 9, თავი " ორგანული ნივთიერებები", ისევე როგორც ქვემოთ).
ნივთიერების ფორმულის წარმოშობის ამოცანების ამოხსნის ალგორითმი.
1. დაასახელეთ ნივთიერების ფორმულა x, y, z და ა.შ. ინდექსების გამოყენებით მოლეკულაში ელემენტების რაოდენობის მიხედვით.
2. თუ ერთი ელემენტის მასური წილი არ არის მოცემული პირობით, გამოთვალეთ იგი, როგორც სხვაობა 100%-სა და ყველა სხვა ელემენტის მასურ წილადებს შორის.
3. იპოვეთ x: y: z ინდექსების შეფარდება, როგორც კოეფიციენტების შეფარდება მასობრივი ფრაქციაელემენტი მისი ფარდობითი ატომური მასით. გადააქციეთ გაყოფის კოეფიციენტები მთელი რიცხვების შეფარდებაზე. განსაზღვრეთ ნივთიერების უმარტივესი ფორმულა.
4. ფორმულების პოვნის პრობლემებში ორგანული ნივთიერებებიხშირად საჭიროა უმარტივესი ფორმულის ფარდობითი მოლეკულური მასის შედარება პრობლემის მდგომარეობის მიხედვით ნაპოვნი ჭეშმარიტის M r-თან (ყველაზე ხშირად სიმკვრივე ჰაერში ან წყალბადში). ამ მასების თანაფარდობა იძლევა რიცხვს, რომლითაც უნდა გამრავლდეს უმარტივესი ფორმულის ინდექსები.
მაგალითი. 15 წყალბადის ორთქლის სიმკვრივის ნახშირწყალბადი შეიცავს 80,0% ნახშირბადს. იპოვეთ მისი მოლეკულური ფორმულა.
მოცემულია: გამოსავალი:
ω (C) = 80.0% 1. ავღნიშნოთ ნახშირწყალბადის ფორმულა C x Hy.
Dn 2 (in-va) \u003d 15 2. გამოთვალეთ წყალბადის მასური წილი ნაერთში:
ω (N) = 100% - ω (C) = 100% - 80.0% = 20.0%
ფორმულა - ? 3. იპოვეთ x: y ინდექსების შეფარდება
ω (FROM) ω (N) 80.0 20.0 6.67 20.0
x: y = --- : --- = --- : --- = 6,67: 20 = --- : --- = 1: 3
A r (C) A r (H) 12 1 6.67 6.67
ნაერთის უმარტივესი ფორმულა CH 3.
4. გამოთვალეთ ნახშირწყალბადის ფარდობითი მოლეკულური წონა:
M r (C x H y) \u003d 2 Dn 2 (in-va) \u003d 2 15 \u003d 30
შეადარეთ იგი უმარტივესი ფორმულის ფარდობით მოლეკულურ წონასთან:
M r (CH 3) \u003d 12 + 3 \u003d 15
M r (C x H y) 30
ჩვენ გავარკვიეთ, რომ უმარტივეს ფორმულაში ორივე ელემენტის ატომების რაოდენობა უნდა გაორმაგდეს. ნივთიერების ჭეშმარიტი ფორმულა C 2 H 6.
3. დაფარული მასალის კონსოლიდაცია.
მოსწავლეების მიერ ამ გაკვეთილის მასალის ათვისება ძალზე მნიშვნელოვანია, ვინაიდან ეს არის ორგანული ნაერთების სხვა კლასის ნომენკლატურისა და იზომერიზმის წარმატებით გააზრების საფუძველი. აუცილებელია საკლასო ოთახში და სახლში დავალებების ძირითადი ტიპების შემუშავება, მხოლოდ ამის შემდეგ შეგიძლიათ გააგრძელოთ შემდგომი მასალის შესწავლა.
სავარჯიშო 1.
1 დონე.
1 . ნახშირწყალბადების შემდეგი ზოგადი ფორმულებიდან რომელი შეესაბამება ალკანებს:
C n H 2n-2; C n H 2n; C n H 2n+2; C n H 2n-6 ?
2 . შეადგინეთ გაჯერებული ნახშირწყალბადების სტრუქტურული ფორმულები მოცემული ნახშირბადის ჩონჩხების მიხედვით:
C – C – C – C C – C C C – C – C – C – C
C-C-C C C-C
C – C – C – C – C
C-C-C C C C
3 . რა ნახშირწყალბადებია ბუტანის ჰომოლოგები: მეთანი, ეთილენი, იზობუტანი, ბენზოლი, პენტანი?
4 . დაწერეთ ნახშირწყალბადების მოლეკულური ფორმულები: პროპანი, ჰექსანი, ოქტანი; რადიკალები: მეთილი, ეთილი,
მე-2 დონე.
1 . მიუთითეთ ალკანების ფორმულები და დაასახელეთ ეს ნივთიერებები:
C 6 H 12, C 4 H 10, C 2 H 6, C 13 H 26, C 6 H 6, C 9 H 20.
2 . ჩამოთვლილი ნახშირწყალბადებიდან რომელი შეიცავს მესამეულ ნახშირბადის ატომს: ეთანი, 2-მეთილბუტანი,
3,3-დიმეთილპენტანი, 2,3-დიმეთილჰექსანი?
3. ჰიბრიდიზაციის რა მდგომარეობაშია ალკანებში ნახშირბადის ყველა ატომი: sp 2 -, sp-, sp 3 - ?
4 . მიუთითეთ ჰომოლოგების წყვილი: ეთანი და ეთილენი; პროპანი და ეთანი; ბუტანი და იზობუტანი; ჰექსანი და ჰეპტანი; მეთანი და
დავალება 2.
1 დონე.
1 . დაწერეთ პენტანის იზომერების სტრუქტურული ფორმულები და დაასახელეთ ისინი.
2 . დაასახელეთ შემდეგი გაჯერებული ნახშირწყალბადები საერთაშორისო ნომენკლატურის მიხედვით:
CH 3 - CH 2 - CH 2 CH 3 - CH - CH 2 - CH - CH 3 CH 3 - CH 2 - CH - CH 2 - CH 3
CH 3 CH 3 CH 3 C 2 H 5
3 . რომელ ალკანებს არ აქვთ იზომერები: მეთანი, ეთანი, პროპანი, ბუტანი?
მე-2 დონე.
1 . დაწერეთ ყველა ჰექსანის იზომერის სტრუქტურული ფორმულები და დაასახელეთ ისინი.
2 . დაწერეთ ყველა ოქტანის იზომერის სტრუქტურული ფორმულები, რომლებსაც აქვთ ერთი მეოთხეული ნახშირბადის ატომი და
დაასახელეთ ისინი.
3 . დაწერეთ სტრუქტურული ფორმულები ალკანის ყველა იზომერისთვის, რომლის ორთქლის სიმკვრივე ჰაერში არის 2,48.
დავალება 3.
დაწერეთ შემდეგი ალკანების სტრუქტურული ფორმულები:
1 დონე. 2-მეთილჰექსანი; 3-მეთილ-3-ეთილპენტანი; 2,3,4 - ტრიმეთილჰექსანი.
მე-2 დონე. 2,2,3,4-ტეტრამეთილჰეპტანი; 2,3-დიმეთილ-3-იზოპროპილჰექსანი; 2-მეთილ-3,3-დიეთილოქტანი.
დავალება 4.
1 დონე.
ერთ-ერთი საბადოს ბუნებრივი აირის კომპონენტების მოცულობითი ფრაქციებია: 92% მეთანი, 5% ეთანი, 2% პროპანი, 0,7% ნახშირბადის მონოქსიდი (IV) და 0,3% აზოტი. განსაზღვრეთ თითოეული ნახშირწყალბადის მოცულობა 120 მ 3 ბუნებრივ აირში.
მე-2 დონე.
ბუნებრივ აირში ალკანების მოცულობითი ფრაქციებია: მეთანი - 91%, ეთანი - 6%, პროპანი - 2%, ბუტანი - 1%. გამოთვალეთ გაზების მასური წილადები და გამოთვალეთ ჰაერის მოცულობა, რომელიც საჭირო იქნება ამ შემადგენლობის 1 მ 3 ბუნებრივი აირის დასაწვავად (ნორმალური პირობები, ჰაერში ჟანგბადის მოცულობითი წილი 20%).
დავალება 5.
1 დონე.
1 . რა პროდუქტები მიიღება C 14 H 30 (ტეტრადეკანი) შემადგენლობის გაჯერებული ნახშირწყალბადის კრეკინგით?
2 . რა ნივთიერებები მიიღება შემდეგი ნივთიერებების ნატრიუმით გაცხელებით: ა) იოდომეთანი;
ბ) 1-ბრომოპროპანი.
3 . დაწერეთ იზომერიზაციის რეაქციის განტოლება ნ-ბუტანი.
4 . რა ნივთიერებები მიიღება ნატრიუმის პროპიონატის CH 3 -CH 2 -COONa ნატრიუმის ჰიდროქსიდით გაცხელებით? დაწერეთ რეაქციის განტოლება.
მე-2 დონე.
1 . დაწერეთ ბზარის განტოლება შემდეგი ალკანებისთვის: ა) ნ-დეკანი; ბ) 2,3-დიმეთილბუტანი.
2 . დაწერეთ ვურცის რეაქციები, რომლებიც შეიძლება გამოყენებულ იქნას შემდეგი ნახშირწყალბადების მისაღებად:
ა) ნ-ჰექსანი; ბ) 2,5-დიმეთილჰექსანი.
3 . ნორმალური სტრუქტურის გაჯერებული ნახშირწყალბადის იზომერიზაციის დროს წარმოიქმნება 2,2,4-ტრიმეთილპენტანი.
განსაზღვრეთ ორიგინალური ნახშირწყალბადი.
4 . შეადგინეთ რეაქციის განტოლებები მარილის გაცხელებით მითითებული ნახშირწყალბადების მისაღებად
შესაბამისი მჟავა ტუტესთან: ა) პროპანი; ბ) 2-მეთილპროპანი.
დავალება 6.
1 დონე.
1. გამოთვალეთ ნახშირბადის მასური წილები ალკანების ჰომოლოგიური სერიის პირველ ოთხ წარმომადგენელში.
2 . განსაზღვრეთ ნახშირწყალბადის ფორმულა, ნახშირბადის მასური წილი, რომელშიც არის 75%, წყალბადი კი 25%.
მე-2 დონე.
1 . გამოთვალეთ წყალბადის მასური წილები ალკანების ჰომოლოგიური სერიის პირველ ოთხ წარმომადგენელში.
გააკეთეთ დასკვნა შემდეგი ჰომოლოგების წყალბადის მასის ფრაქციის შემდგომი ცვლილების შესახებ.
2. ნახშირწყალბადში ნახშირბადის მასური წილი არის 82,76%. ნორმალურ პირობებში 10 ლიტრი ეს გაზი
აქვს მასა 25,88 გ.შეადგინეთ ნახშირწყალბადის იზომერების სტრუქტურული ფორმულები და დაასახელეთ ისინი მიხედვით
საერთაშორისო ნომენკლატურა.
4. Საშინაო დავალება: § 11 გვ.67 - 72, ექს. 1-6 წმ. 81; რეპ. § ათი.
მეთოდური ლიტერატურა
გაბრიელიანი ო.ს., ოსტროუმოვი ი.გ. მასწავლებლის სახელმძღვანელო. Ქიმია. 10 უჯრედი – M.: Bustard, 2004 წ.
გაბრიელიანი O.S., Runov N.N., Tolkunov V.I. ქიმიური ექსპერიმენტი სკოლაში. მე-10 კლასი. M.: Bustard, 2005 წ.
გაბრიელიანი O.S., Popkova T.N., Kartsova A.A. ორგანული ქიმია, 10: პროფილის დონე: მეთოდოლოგიური გზამკვლევი: წიგნი მასწავლებლებისთვის. მ.: განათლება, 2006 წ.
ძმარმჟავას ნატრიუმის მარილის (ნატრიუმის აცეტატის) გათბობა ტუტეების ჭარბი რაოდენობით იწვევს კარბოქსილის ჯგუფის აღმოფხვრას და მეთანის წარმოქმნას:
CH3CONa + NaOH CH4 + Na2CO3
თუ ნატრიუმის აცეტატის ნაცვლად ვიღებთ ნატრიუმის პროპიონატს, მაშინ წარმოიქმნება ეთანი, ნატრიუმის ბუტანოატისგან - პროპანი და ა.შ.
RCH2CONa + NaOH -> RCH3 + Na2CO3
5. ვურცის სინთეზი. როდესაც ჰალოალკანები რეაგირებს ტუტე მეტალის ნატრიუმთან, წარმოიქმნება გაჯერებული ნახშირწყალბადები და ტუტე ლითონის ჰალოიდი, მაგალითად:
ტუტე ლითონის მოქმედება ჰალოკარბონების ნარევზე (მაგ. ბრომოეთანი და ბრომმეთანი) გამოიწვევს ალკანების (ეთანი, პროპანი და ბუტანი) ნარევის წარმოქმნას.
რეაქცია, რომელზედაც დაფუძნებულია ვურცის სინთეზი, კარგად მიმდინარეობს მხოლოდ ჰალოალკანებთან, რომელთა მოლეკულებში ჰალოგენის ატომი მიმაგრებულია ნახშირბადის პირველად ატომთან.
6. კარბიდების ჰიდროლიზი. ნახშირბადის შემცველი ზოგიერთი კარბიდის დამუშავებისას -4 დაჟანგვის მდგომარეობაში (მაგალითად, ალუმინის კარბიდი), წყალთან ერთად წარმოიქმნება მეთანი:
Al4C3 + 12H20 = ZCH4 + 4Al(OH)3 ფიზიკური თვისებები
მეთანის ჰომოლოგიური სერიის პირველი ოთხი წარმომადგენელი არის აირები. მათგან უმარტივესი არის მეთანი - უფერო, უგემოვნო და უსუნო გაზი („გაზის“ სუნი, რომელსაც უნდა დარეკოთ 04, განისაზღვრება მერკაპტანების სუნით - გოგირდის შემცველი ნაერთები, რომლებიც სპეციალურად ემატება მეთანს, რომელიც გამოიყენება საყოფაცხოვრებო პირობებში. და სამრეწველო გაზის მოწყობილობები, რათა მათთან ახლოს მყოფმა ადამიანებმა იგრძნონ გაჟონვის სუნი).
C5H12-დან C15H32-მდე შემადგენლობის ნახშირწყალბადები სითხეებია, მძიმე ნახშირწყალბადები მყარია.
ალკანების დუღილის და დნობის წერტილები თანდათან იზრდება ნახშირბადის ჯაჭვის სიგრძის მატებასთან ერთად. ყველა ნახშირწყალბადები ცუდად ხსნადია წყალში; თხევადი ნახშირწყალბადები ჩვეულებრივი ორგანული გამხსნელებია.
ქიმიური თვისებები
1. ჩანაცვლების რეაქციები. ალკანებისთვის ყველაზე დამახასიათებელია თავისუფალი რადიკალების შემცვლელი რეაქციები, რომლის დროსაც წყალბადის ატომი იცვლება ჰალოგენის ატომით ან რომელიმე ჯგუფით.
წარმოგიდგენთ ყველაზე ტიპიური რეაქციების განტოლებებს.
ჰალოგენაცია:
CH4 + C12 -> CH3Cl + HCl
ჰალოგენის სიჭარბის შემთხვევაში, ქლორირება შეიძლება უფრო შორს წავიდეს, წყალბადის ყველა ატომის ქლორით ჩანაცვლებამდე:
CH3Cl + C12 -> HCl + CH2Cl2
დიქლორმეთანის მეთილენქლორიდი
CH2Cl2 + Cl2 -> HCl + CHCl3
ტრიქლორმეთანის ქლოროფორმი
CHCl3 + Cl2 -> HCl + CCl4
ნახშირბადის ტეტრაქლორიდი ნახშირბადის ტეტრაქლორიდი
მიღებული ნივთიერებები ფართოდ გამოიყენება როგორც გამხსნელები და საწყისი მასალები ორგანულ სინთეზში.
2. დეჰიდროგენაცია (წყალბადის ელიმინაცია). როდესაც ალკანები გადადიან კატალიზატორზე (Pt, Ni, A12O3, Cr2O3) მაღალ ტემპერატურაზე (400-600 °C), წყალბადის მოლეკულა იშლება და წარმოიქმნება ალკენი:
CH3-CH3 -> CH2=CH2 + H2
3. რეაქციები, რომელსაც თან ახლავს ნახშირბადის ჯაჭვის განადგურება. ყველა გაჯერებული ნახშირწყალბადი იწვის ნახშირორჟანგის და წყლის წარმოქმნით. აირისებრი ნახშირწყალბადები, რომლებიც შერეულია ჰაერთან გარკვეული პროპორციებით, შეიძლება აფეთქდეს. გაჯერებული ნახშირწყალბადების წვა არის თავისუფალი რადიკალების ეგზოთერმული რეაქცია, რომელსაც დიდი მნიშვნელობა აქვს ალკანების საწვავად გამოყენებისას.
CH4 + 2O2 -> CO2 + 2H2O + 880 კჯ
ზოგადად, ალკანების წვის რეაქცია შეიძლება დაიწეროს შემდეგნაირად:

თერმული გაყოფის რეაქციები საფუძვლად უდევს სამრეწველო პროცესს - ნახშირწყალბადების კრეკინგი. ეს პროცესი ნავთობის გადამუშავების ყველაზე მნიშვნელოვანი ეტაპია.
როდესაც მეთანი თბება 1000 ° C ტემპერატურამდე, იწყება მეთანის პიროლიზი - დაშლა მარტივ ნივთიერებებად. 1500 ° C ტემპერატურაზე გაცხელებისას შესაძლებელია აცეტილენის წარმოქმნა.
4. იზომერიზაცია. როდესაც ხაზოვანი ნახშირწყალბადები თბება იზომერიზაციის კატალიზატორით (ალუმინის ქლორიდი), წარმოიქმნება ნივთიერებები განშტოებული ნახშირბადის ჩონჩხით: 
5. არომატიზაცია. ალკანები ექვსი ან მეტი ნახშირბადის ატომით ჯაჭვში კატალიზატორის თანდასწრებით ციკლირდება ბენზოლისა და მისი წარმოებულების წარმოქმნით: 
რა არის მიზეზი იმისა, რომ ალკანები შედიან რეაქციებში, რომლებიც მიმდინარეობს თავისუფალი რადიკალების მექანიზმის მიხედვით? ალკანის მოლეკულებში ნახშირბადის ყველა ატომი sp 3 ჰიბრიდიზაციის მდგომარეობაშია. ამ ნივთიერებების მოლეკულები აგებულია კოვალენტური არაპოლარული C-C (ნახშირბადი-ნახშირბადი) ბმებისა და სუსტად პოლარული C-H (ნახშირბადი-წყალბადის) ბმების გამოყენებით. მათ არ აქვთ გაზრდილი და შემცირებული ელექტრონის სიმკვრივის მქონე უბნები, ადვილად პოლარიზებადი ბმები, ანუ ისეთი ბმები, რომლებშიც ელექტრონის სიმკვრივე შეიძლება გადაინაცვლოს გარე გავლენის გავლენის ქვეშ (იონების ელექტროსტატიკური ველები). შესაბამისად, ალკანები არ რეაგირებენ დამუხტულ ნაწილაკებთან, ვინაიდან ალკანის მოლეკულებში ბმები ჰეტეროლიზური მექანიზმით არ იშლება.
ალკანების ყველაზე დამახასიათებელი რეაქციებია თავისუფალი რადიკალების ჩანაცვლების რეაქციები. ამ რეაქციების დროს წყალბადის ატომი იცვლება ჰალოგენის ატომით ან რომელიმე ჯგუფით.
თავისუფალი რადიკალების ჯაჭვური რეაქციების კინეტიკა და მექანიზმი, ანუ რეაქციები, რომლებიც წარმოიქმნება თავისუფალი რადიკალების მოქმედებით - ნაწილაკები დაუწყვილებელი ელექტრონებით - შეისწავლა გამოჩენილი რუსი ქიმიკოსი ნ.ნ. სემენოვი. სწორედ ამ კვლევებისთვის მიენიჭა ნობელის პრემია ქიმიაში.
ჩვეულებრივ, თავისუფალი რადიკალების ჩანაცვლების რეაქციის მექანიზმი წარმოდგენილია სამი ძირითადი ეტაპით:
1. ინიცირება (ჯაჭვის ბირთვი, თავისუფალი რადიკალების წარმოქმნა ენერგიის წყაროს მოქმედებით - ულტრაიისფერი შუქი, გათბობა).
2. ჯაჭვის განვითარება (თავისუფალი რადიკალების და არააქტიური მოლეკულების თანმიმდევრული ურთიერთქმედების ჯაჭვი, რის შედეგადაც წარმოიქმნება ახალი რადიკალები და ახალი მოლეკულები).
3. ჯაჭვის შეწყვეტა (თავისუფალი რადიკალების შერწყმა არააქტიურ მოლეკულებად (რეკომბინაცია), რადიკალების „სიკვდილი“, რეაქციების ჯაჭვის შეწყვეტა).
სამეცნიერო კვლევა ნ.ნ. სემენოვი
სემენოვი ნიკოლაი ნიკოლაევიჩი
(1896 - 1986)

საბჭოთა ფიზიკოსი და ფიზიკოსი, აკადემიკოსი. ლაურეატი ნობელის პრემია(1956). სამეცნიერო კვლევა ეხება დოქტრინას ქიმიური პროცესების, კატალიზის, ჯაჭვური რეაქციების, თერმული აფეთქებისა და გაზის ნარევების წვის თეორიას.
განვიხილოთ ეს მექანიზმი მეთანის ქლორირების რეაქციის მაგალითის გამოყენებით:
CH4 + Cl2 -> CH3Cl + HCl
ჯაჭვის დაწყება ხდება იმის შედეგად, რომ ულტრაიისფერი გამოსხივების ან გაცხელების გავლენის ქვეშ ხდება Cl-Cl ბმის ჰომლიზური გაყოფა და ქლორის მოლეკულა იშლება ატომებად:
Cl: Cl -> Cl + + Cl
შედეგად მიღებული თავისუფალი რადიკალები თავს ესხმიან მეთანის მოლეკულებს, ანადგურებენ მათ წყალბადის ატომს:
CH4 + Cl -> CH3 + HCl
და გარდაიქმნება CH3 რადიკალებად, რომლებიც, თავის მხრივ, ქლორის მოლეკულებთან შეჯახებით, ანადგურებენ მათ ახალი რადიკალების წარმოქმნით:
CH3 + Cl2 -> CH3Cl + Cl და ა.შ.
ჯაჭვი ვითარდება.
რადიკალების წარმოქმნასთან ერთად, მათი "სიკვდილი" ხდება რეკომბინაციის პროცესის შედეგად - ორი რადიკალისგან არააქტიური მოლეკულის წარმოქმნა:
CH3 + Cl -> CH3Cl
Cl+ + Cl+ -> Cl2
CH3 + CH3 -> CH3-CH3
საინტერესოა აღინიშნოს, რომ რეკომბინაციის დროს გამოიყოფა ზუსტად იმდენი ენერგია, რამდენიც საჭიროა ახლად წარმოქმნილი ბმის გასანადგურებლად. ამასთან დაკავშირებით, რეკომბინაცია შესაძლებელია მხოლოდ იმ შემთხვევაში, თუ ორი რადიკალის შეჯახება მოიცავს მესამე ნაწილაკს (სხვა მოლეკულა, რეაქციის ჭურჭლის კედელი), რომელიც იღებს ზედმეტ ენერგიას. ეს შესაძლებელს ხდის თავისუფალი რადიკალების ჯაჭვური რეაქციების რეგულირებას და შეჩერებას.
ყურადღება მიაქციეთ რეკომბინაციის რეაქციის ბოლო მაგალითს - ეთანის მოლეკულის წარმოქმნას. ეს მაგალითი აჩვენებს, რომ რეაქცია ორგანულ ნაერთებთან ერთად საკმაოდ რთული პროცესია, რომელიც ძირითად რეაქციის პროდუქტთან ერთად ხშირად იწვევს ქვეპროდუქტების წარმოქმნას, რაც იწვევს გაწმენდისა და იზოლაციის რთული და ძვირადღირებული მეთოდების შემუშავების აუცილებლობას. სამიზნე ნივთიერებები.
მეთანის ქლორირებით მიღებული სარეაქციო ნაზავი ქლორმეთანთან (CH3Cl) და წყალბადის ქლორიდთან ერთად შეიცავს: დიქლორმეთანს (CH2Cl2), ტრიქლორმეთანს (CHCl3), ნახშირბადის ტეტრაქლორიდს (CCl4), ეთანს და მის ქლორირების პროდუქტებს.
ახლა შევეცადოთ განვიხილოთ უფრო რთული ორგანული ნაერთის - პროპანის ჰალოგენაციის რეაქცია (მაგალითად, ბრომიაცია).
თუ მეთანის ქლორირების შემთხვევაში შესაძლებელია მხოლოდ ერთი მონოქლორის წარმოებული, მაშინ ამ რეაქციაში უკვე შეიძლება წარმოიქმნას ორი მონობრომული წარმოებული: 
ჩანს, რომ პირველ შემთხვევაში წყალბადის ატომი იცვლება პირველად ნახშირბადის ატომზე, ხოლო მეორე შემთხვევაში მეორადში. ამ რეაქციების სიჩქარე იგივეა? გამოდის, რომ საბოლოო ნარევში ჭარბობს წყალბადის ატომის ჩანაცვლების პროდუქტი, რომელიც მდებარეობს მეორად ნახშირბადზე, ანუ 2-ბრომოპროპანი (CH3-CHBr-CH3). შევეცადოთ ავხსნათ ეს.
ამისათვის ჩვენ უნდა გამოვიყენოთ შუალედური ნაწილაკების სტაბილურობის იდეა. შენიშნეთ, რომ მეთანის ქლორირების რეაქციის მექანიზმის აღწერისას ჩვენ ვახსენეთ მეთილის რადიკალი - CH3? ეს რადიკალი არის შუალედური ნაწილაკი მეთან CH4-სა და ქლორმეთანს CH3Cl-ს შორის. შუალედური ნაწილაკი პროპანსა და 1-ბრომოპროპანს შორის არის რადიკალი დაუწყვილებელი ელექტრონით პირველად ნახშირბადთან, ხოლო პროპანსა და 2-ბრომოპროპანს შორის - მეორადში.
მეორადი ნახშირბადის ატომზე დაუწყვილებელი ელექტრონის მქონე რადიკალი (b) უფრო სტაბილურია, ვიდრე თავისუფალი რადიკალი დაუწყვილებელი ელექტრონით პირველად ნახშირბადის ატომზე (a). იგი ჩამოყალიბებულია მეტი. ამ მიზეზით, პროპან ბრომირების რეაქციის მთავარი პროდუქტია 2-ბრომო-პროპანი, ნაერთი, რომლის წარმოქმნა მიმდინარეობს უფრო სტაბილური შუალედური ნაწილაკების მეშვეობით.
აქ მოცემულია თავისუფალი რადიკალების რეაქციების რამდენიმე მაგალითი:
ნიტრაციის რეაქცია (კონოვალოვის რეაქცია) ![]()
რეაქცია გამოიყენება ნიტრო ნაერთების - გამხსნელების, მრავალი სინთეზისთვის საწყისი მასალების მისაღებად.
ალკანების კატალიზური დაჟანგვა ჟანგბადით
ეს რეაქციები არის ყველაზე მნიშვნელოვანი სამრეწველო პროცესების საფუძველი გაჯერებული ნახშირწყალბადებისგან უშუალოდ ალდეჰიდების, კეტონების, ალკოჰოლების მისაღებად, მაგალითად:
CH4 + [O] -> CH3OH
განაცხადი
გაჯერებული ნახშირწყალბადები, განსაკუთრებით მეთანი, ფართოდ გამოიყენება ინდუსტრიაში (სქემა 2). ისინი წარმოადგენენ მარტივ და საკმაოდ იაფ საწვავს, ნედლეულს დიდი რაოდენობით ყველაზე მნიშვნელოვანი ნაერთების მისაღებად.
მეთანისგან მიღებული ნაერთები, ყველაზე იაფი ნახშირწყალბადის საკვები მასალა, გამოიყენება მრავალი სხვა ნივთიერებისა და მასალის წარმოებისთვის. მეთანი გამოიყენება როგორც წყალბადის წყარო ამიაკის სინთეზში, ასევე სინთეზური აირის (CO და H2 ნარევი) წარმოებისთვის, რომელიც გამოიყენება ნახშირწყალბადების, ალკოჰოლების, ალდეჰიდების და სხვა ორგანული ნაერთების სამრეწველო სინთეზისთვის. 
უფრო მაღალი დუღილის ნავთობის ფრაქციების ნახშირწყალბადები გამოიყენება როგორც საწვავი დიზელის და ტურბორეაქტიული ძრავებისთვის, როგორც საპოხი ზეთების ბაზა, როგორც ნედლეული სინთეზური ცხიმების წარმოებისთვის და ა.შ.
აქ მოცემულია რამდენიმე ინდუსტრიულად მნიშვნელოვანი რეაქცია მეთანთან დაკავშირებით. მეთანი გამოიყენება ქლოროფორმის, ნიტრომეთანის, ჟანგბადის შემცველი წარმოებულების წარმოებისთვის. ალკოჰოლები, ალდეჰიდები, კარბოქსილის მჟავები შეიძლება წარმოიქმნას ალკანების პირდაპირი ურთიერთქმედებით ჟანგბადთან, რეაქციის პირობებიდან გამომდინარე (კატალიზატორი, ტემპერატურა, წნევა): 
როგორც უკვე იცით, C5H12-დან C11H24-მდე შემადგენლობის ნახშირწყალბადები შედის ნავთობის ბენზინის ფრაქციაში და ძირითადად გამოიყენება როგორც საწვავი შიდა წვის ძრავებისთვის. ცნობილია, რომ ბენზინის ყველაზე ღირებული კომპონენტებია იზომერული ნახშირწყალბადები, რადგან მათ აქვთ ყველაზე მაღალი დარტყმის წინააღმდეგობა.
ნახშირწყალბადები ატმოსფერულ ჟანგბადთან შეხებისას ნელ-ნელა ქმნიან მასთან ნაერთებს - პეროქსიდებს. ეს არის ნელი თავისუფალი რადიკალების რეაქცია, რომელიც იწყება ჟანგბადის მოლეკულით: 
გაითვალისწინეთ, რომ ჰიდროპეროქსიდის ჯგუფი იქმნება ნახშირბადის მეორად ატომებზე, რომლებიც ყველაზე მრავლადაა ხაზოვან ან ნორმალურ ნახშირწყალბადებში.
წნევისა და ტემპერატურის მკვეთრი მატებით, რაც ხდება შეკუმშვის ინსულტის ბოლოს, ამ პეროქსიდის ნაერთების დაშლა იწყება დიდი რაოდენობით თავისუფალი რადიკალების წარმოქმნით, რომლებიც „იწყებენ“ თავისუფალი რადიკალების წვის ჯაჭვურ რეაქციას საჭიროზე ადრე. . დგუში კვლავ მაღლა მიდის და ბენზინის წვის პროდუქტები, რომლებიც უკვე წარმოიქმნება ნარევის ნაადრევი აალების შედეგად, მას ქვევით უბიძგებს. ეს იწვევს ძრავის სიმძლავრის მკვეთრ შემცირებას, მის ცვეთას.
ამრიგად, დეტონაციის მთავარი მიზეზი არის პეროქსიდის ნაერთების არსებობა, რომლის ფორმირების უნარი მაქსიმალურია ხაზოვანი ნახშირწყალბადებისთვის.
კ-ჰეპტანს აქვს ყველაზე დაბალი დეტონაციის წინააღმდეგობა ბენზინის ფრაქციის ნახშირწყალბადებს შორის (C5H14 - C11H24). ყველაზე სტაბილური (ანუ წარმოქმნის პეროქსიდებს ყველაზე ნაკლებად) არის ეგრეთ წოდებული იზოოქტანი (2,2,4-ტრიმეთილპენტანი).
ბენზინის დარტყმის წინააღმდეგობის ზოგადად მიღებული მახასიათებელია ოქტანური რიცხვი. ოქტანური მაჩვენებელი 92 (მაგალითად, A-92 ბენზინი) ნიშნავს, რომ ამ ბენზინს აქვს იგივე თვისებები, რაც ნარევი, რომელიც შედგება 92% იზოოქტანისა და 8% ჰეპტანისგან.
დასასრულს, შეიძლება დავამატოთ, რომ მაღალი ოქტანის ბენზინის გამოყენება შესაძლებელს ხდის შეკუმშვის კოეფიციენტის გაზრდას (ზეწოლა შეკუმშვის ინსულტის ბოლოს), რაც იწვევს შიდა წვის ძრავის სიმძლავრისა და ეფექტურობის ზრდას.
ბუნებაში ყოფნა და მიღება
დღევანდელ გაკვეთილზე თქვენ გაეცანით ისეთ კონცეფციას, როგორიცაა ალკანები და ასევე შეიტყვეთ ამის შესახებ. ქიმიური შემადგენლობადა მიღების მეთოდები. ამიტომ, მოდით, ახლა უფრო დეტალურად ვისაუბროთ ბუნებაში ალკანების პოვნის თემაზე და გავარკვიოთ, როგორ და სად იპოვეს ალკანებმა გამოყენება.
ალკანების მიღების ძირითადი წყაროა ბუნებრივი აირი და ნავთობი. ისინი შეადგენენ ნავთობის გადამუშავების პროდუქტების დიდ ნაწილს. მეთანი, რომელიც გავრცელებულია დანალექი ქანების საბადოებში, ასევე არის ალკანების გაზის ჰიდრატი.
ბუნებრივი აირის ძირითადი კომპონენტია მეთანი, მაგრამ ის ასევე შეიცავს ეთანს, პროპანს და ბუტანს მცირე რაოდენობით. მეთანი გვხვდება ქვანახშირის ნაკერების ემისიებში, ჭაობებში და მათთან დაკავშირებულ ნავთობის აირებში.
ანკანის მიღება შესაძლებელია ნახშირის კოქსირებითაც. ბუნებაში ასევე გვხვდება ეგრეთ წოდებული მყარი ალკანები - ოზოცერიტები, რომლებიც წარმოდგენილია მთის ცვილის საბადოების სახით. ოზოკერიტი გვხვდება მცენარეების ცვილის ფენებში ან მათ თესლებში, ასევე ფუტკრის შემადგენლობაში.
ალკანების სამრეწველო იზოლაცია აღებულია ბუნებრივი წყაროებიდან, რომლებიც, საბედნიეროდ, ჯერ კიდევ ამოუწურავია. ისინი მიიღება ნახშირბადის ოქსიდების კატალიზური ჰიდროგენაციით. ასევე, მეთანის მიღება შესაძლებელია ლაბორატორიაში ნატრიუმის აცეტატის მყარი ტუტეთ გაცხელების ან ზოგიერთი კარბიდის ჰიდროლიზის მეთოდით. მაგრამ ასევე ალკანების მიღება შესაძლებელია კარბოქსილის მჟავების დეკარბოქსილირებით და მათი ელექტროლიზით.
ალკანების გამოყენება
საყოფაცხოვრებო დონეზე ალკანები ფართოდ გამოიყენება ადამიანის საქმიანობის მრავალ სფეროში. ძნელი წარმოსადგენია ჩვენი ცხოვრება ბუნებრივი აირის გარეშე. და არავისთვის არ იქნება საიდუმლო, რომ ბუნებრივი აირის საფუძველია მეთანი, საიდანაც წარმოიქმნება ნახშირბადი, რომელიც გამოიყენება ტოპოგრაფიული საღებავებისა და საბურავების წარმოებაში. მაცივარი, რომელიც ყველას აქვს სახლში, ასევე მუშაობს მაცივრად გამოყენებული ალკანური ნაერთების წყალობით. ხოლო მეთანისგან მიღებული აცეტილენი გამოიყენება ლითონების შესადუღებლად და დასაჭრელად.
ახლა უკვე იცით, რომ ალკანები საწვავად გამოიყენება. ისინი წარმოდგენილია ბენზინის, ნავთის, მზის ზეთისა და მაზუთის შემადგენლობაში. გარდა ამისა, ისინი ასევე შედიან საპოხი ზეთების, ნავთობის ჟელესა და პარაფინის შემადგენლობაში.
როგორც გამხსნელი და სხვადასხვა პოლიმერების სინთეზისთვის, ციკლოჰექსანმა იპოვა ფართო გამოყენება. ციკლოპროპანი გამოიყენება ანესთეზიის დროს. Squalane, როგორც მაღალი ხარისხის საპოხი ზეთი, არის მრავალი ფარმაცევტული და კოსმეტიკური პრეპარატის ინგრედიენტი. ალკანები არის ნედლეული, რომლითაც მიიღება ორგანული ნაერთები, როგორიცაა ალკოჰოლი, ალდეჰიდები და მჟავები.
პარაფინი არის უმაღლესი ალკანების ნარევი და რადგან ის არატოქსიკურია, ფართოდ გამოიყენება Კვების ინდუსტრია. იგი გამოიყენება რძის პროდუქტების, წვენების, მარცვლეულის და ა.შ. პაკეტების გაჟღენთისთვის, ასევე საღეჭი რეზინის წარმოებაში. გაცხელებულ პარაფინს კი მედიცინაში იყენებენ პარაფინის სამკურნალოდ.
გარდა ზემოაღნიშნულისა, ასანთის თავები გაჟღენთილია პარაფინით, მათი უკეთ დასაწვავად მისგან მზადდება ფანქრები და სანთლები.
პარაფინის დაჟანგვით მიიღება ჟანგბადის შემცველი პროდუქტები, ძირითადად ორგანული მჟავები. ნახშირწყალბადის გარკვეული რაოდენობის ნახშირწყალბადების შერევისას მიიღება ნავთობის ჟელე, რომელმაც ფართო გამოყენება ჰპოვა როგორც პარფიუმერიაში, ასევე კოსმეტოლოგიაში და მედიცინაში. გამოიყენება სხვადასხვა მალამოების, კრემებისა და გელების მოსამზადებლად. და ასევე გამოიყენება მედიცინაში თერმული პროცედურებისთვის.
პრაქტიკული დავალებები
1. ჩამოწერეთ ალკანების ჰომოლოგიური რიგის ნახშირწყალბადების ზოგადი ფორმულა.
2. დაწერეთ ჰექსანის შესაძლო იზომერების ფორმულები და დაასახელეთ სისტემატური ნომენკლატურის მიხედვით.
3. რა არის კრეკინგი? რა სახის კრეკი იცით?
4. დაწერეთ ფორმულები ჰექსანის კრეკინგის შესაძლო პროდუქტებისთვის.
5. გაშიფრეთ გარდაქმნების შემდეგი ჯაჭვი. დაასახელეთ ნაერთები A, B და C.
6. მიეცით ნახშირწყალბადის C5H12 სტრუქტურული ფორმულა, რომელიც ბრომირებისას ქმნის მხოლოდ ერთ მონობრომ წარმოებულს.
7. უცნობი აგებულების ალკანის 0,1 მოლი სრული წვისთვის დაიხარჯა 11,2 ლიტრი ჟანგბადი (ნ.ა.). რა არის ალკანის სტრუქტურული ფორმულა?
8. როგორია აირისებრი გაჯერებული ნახშირწყალბადის სტრუქტურული ფორმულა, თუ ამ აირის 11 გ იკავებს 5,6 ლიტრ მოცულობას (ნ.ა.)?
9. გადახედეთ რა იცით მეთანის გამოყენების შესახებ და ახსენით, რატომ არის საყოფაცხოვრებო გაზის გაჟონვის დადგენა სუნით, თუმცა მისი შემადგენელი კომპონენტები უსუნოა.
ათი *. რა ნაერთების მიღება შეიძლება მეთანის კატალიზური დაჟანგვით სხვადასხვა პირობებში? დაწერეთ შესაბამისი რეაქციების განტოლებები.
თერთმეტი*. სრული წვის პროდუქტები (ჟანგბადის ჭარბი რაოდენობით) 10,08 ლიტრი (ნ.ა.) ეთანისა და პროპანის ნარევი გადატანილია ჭარბი ცაცხვის წყალში. ამან წარმოქმნა 120 გრ ნალექი. განსაზღვრეთ საწყისი ნარევის მოცულობითი შემადგენლობა.
12*. ორი ალკანის ნარევის ეთანის სიმკვრივეა 1,808. ამ ნარევის ბრომირებისას იზოლირებული იყო მხოლოდ ორი წყვილი იზომერული მონობრომოალკანები. მსუბუქი იზომერების ჯამური მასა რეაქციის პროდუქტებში უდრის უფრო მძიმე იზომერების საერთო მასას. განსაზღვრეთ უფრო მძიმე ალკანის მოცულობითი წილი საწყის ნარევში.















